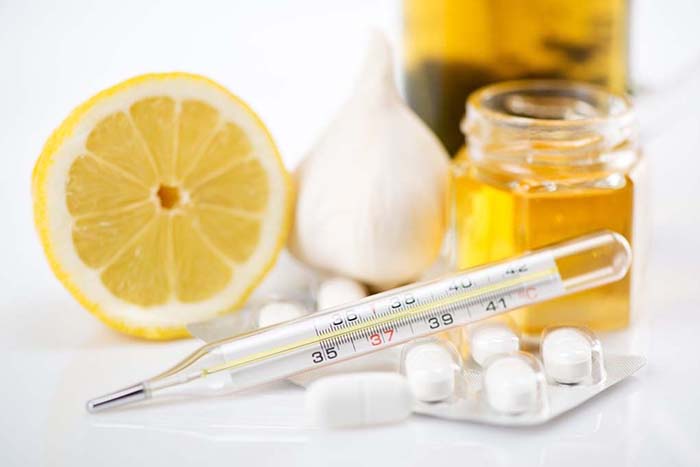
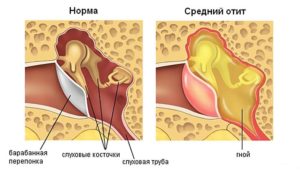
Препараты интерферона
Содержание:
- Краткая инструкция по применению и переносимости препаратов с содержанием интерферона альфа-2б
- Действительно ли Интерферон при коронавирусе поможет
- Преимущества ректальной формы ИФН с точки зрения фармакокинетических параметров
- Криданимод
- Интерферон лейкоцитарный человеческий
- Виды искусственных интерферонов
- Показания к применению интерферона
- Способы получения интерферонов, классификация
- Клинико-фармакологические аспекты преимуществ комбинации ИФН с антиоксидантами. Фармакокинетическое взаимодействие
- Какие препараты интерферона лучше выбрать
- Преимущество индукторов эндогенного протеина
- Применение Интерферона
Краткая инструкция по применению и переносимости препаратов с содержанием интерферона альфа-2б
Признание научным сообществом
Интерферон альфа-2b (ВИФЕРОН) включен в три федеральных стандарта оказания медицинской помощи как рекомендованный препарат для лечения гриппа и ОРВИ, а также в три Федеральных Протокола лечения этих заболеваний.1 Если принимать во внимание не только грипп и ОРВИ, но и другие заболевания, то количество стандартов и рекомендаций касаемо этого препарата еще больше – интерферон (ВИФЕРОН) включен в 30 федеральных стандартов оказания медицинской помощи взрослым и детям, утвержденных Минздравом РФ, а также в 21 Протокол (Клинические рекомендации) оказания медицинской помощи взрослым, в том числе беременным женщинам, и детям
Принцип действия препарата
Интерферон альфа-2b человеческий рекомбинантный, входящий в состав препарата ВИФЕРОН, обладает противовирусными, иммуномодулирующими свойствами и подавляет репликацию РНК- и ДНК-содержащих вирусов. К противовирусной терапии против гриппа можно приступить на любой фазе заболевания. Это поможет улучшить состояние и предотвратить развитие осложнений2. В препарат ВИФЕРОН входят общепризнанные высокоактивные антиоксиданты: в свечах это витамины Е и С, в мази – витамин Е, в геле – витамин Е, лимонная и бензойная кислоты. На фоне такой антиоксидантной поддержки отмечается повышение противовирусной активности интерферонов.
Результаты испытаний препарата

ВИФЕРОН прошел полный цикл клинических испытаний при широком спектре различных заболеваний в ведущих клиниках России. Результатом проведенных исследований явилось доказательство лечебно-профилактической эффективности препарата ВИФЕРОН при различных инфекционно-воспалительных заболеваниях у взрослых и детей, включая новорожденных, и беременных женщин. Научно доказано, что комплексный состав и форма выпуска обеспечивает препарату ВИФЕРОН уникальные фармакокинетические характеристики, с пролонгированием действия интерферона при отсутствии побочных эффектов, присущих парентеральным препаратам рекомбинантных интерферонов3.
При каких заболеваниях применяются препараты на основе интерферона alpha-2b
Препарат ВИФЕРОН в виде суппозиториев, геля и мази применяется для лечения следующих заболеваний:
- ОРВИ, в том числе грипп;
- герпес;
- папилломавирусная инфекция;
- цитомегаловирусная инфекция;
- энтеровирусная инфекция;
- ларинготрахеобронхит;
- хронические гепатиты В, С, D, включая осложненные циррозом печени;
- бактериальный вагиноз;
- кандидоз;
- микоплазмоз;
- уреаплазмоз;
- гарднереллез.
Применение препарата ВИФЕРОН в составе комплексной противовирусной терапии позволяет снизить терапевтические дозы антибактериальных и гормональных лекарственных средств, а также уменьшить токсические эффекты указанной терапии.
Автор статьи
Врач общей практики
- http://www.rosminzdrav.ru, Приказ Министерства здравоохранения Российской Федерации, http://www.raspm.ru; http://www.niidi.ru; http://www.pediatr-russia.ru; http://www.nnoi.ru
- Нестерова И.В. «Препараты интерферона в клинической практике: когда и как», «Лечащий врач», сентябрь 2017.
- «ВИФЕРОН – комплексный противовирусный и иммуномодулирующий препарат для лечения инфекционно-воспалительных заболеваний в перинатологии». (Руководство для врачей), Москва, 2014.
Действительно ли Интерферон при коронавирусе поможет
Пока нет широкомасштабных клинических исследований, которые смогли бы установить самый эффективный препарат при коронавирусе, но есть предположение, что поможет Интерферон. Оно основано, как и все другие способы лечения, на прошлом опыте.
Так, швейцарскими учеными он был использован в 2003 году при лечении эпидемической вспышки острой респираторной инфекции (ТОРС-синдрома). Она была вызвана похожим коронавирусом, ранее поражавшим летучих мышей. Этот штамм, как и COVID-19, взаимодействовал с рецепторами для ангиотензина 2 и подавлял при развитии инфекции образование собственного интерферона. Эту особенность ученые считали одной из причин тяжелого течения инфекции.
При введении препаратов с рекомбинантным Интерфероном (полученным искусственным путем) уменьшалась способность прикрепления коронавируса к оболочкам клеток, что снижало восприимчивость к заражению. Именно это свойство было положено в основу рекомендаций по профилактике инфекции при помощи Интерферона. Сходные данные были получены в 2012 году при развитии эпидемии MERS-CoV.
Механизм противовирусного действия медикамента основан на том, что он запускает образование фермента (протеинкиназы) внутри клеток, который может остановить размножение вирусного белка и РНК-азы, помогающей разрушить РНК коронавируса. Этот препарат также:
- меняет свойства клеточной мембраны, что предупреждает проникновение вируса внутрь клетки;
- стимулирует активность Т-лимфоцитов, которые разрушают клетки, зараженные коронавирусами.
Почему некоторые ученые не рекомендуют его
Не все ученые придерживаются мнения, что при коронавирусе Интерферон будет спасением, они не рекомендуют его применение, так как:
- нет исследований, отвечающих всем требованиям, проведенных при текущей пандемии;
- препарат максимально эффективен при начальных признаках, если же начать его принимать самостоятельно в разгар болезни, то можно получить более тяжелую форму (хотя такая реакция типична для инъекционной формы и больших доз);
- реальный эффект в распространении коронавируса может иметь вакцина, так как у населения нет приобретенного иммунитета к новому возбудителю инфекции.
Какой Интерферон лучше для лечения: альфа, бета, гамма
Противовирусное действие в большей степени проявляет интерферон альфа и бета, а для гамма-интерферона характерно стимулирующее влияние на клетки иммунной системы, что может быть не всегда желательным эффектом. Поэтому в рекомендациях Минздрава есть указание о применении интерферона альфа 2b против коронавируса для профилактики заражения.
Какие препараты Интерферона эффективны
Со времени появления рекомбинантного интерферона, который получен из кишечной палочки (в нее поместили соответствующий ген), ему отдается предпочтение. При этом предыдущий препарат (Интерферон лейкоцитарный человеческий жидкий) утратил свою популярность, и рекомендаций о его применении от коронавируса пока нет.
Преимущества ректальной формы ИФН с точки зрения фармакокинетических параметров
Являясь белками, ИФН разрушаются в желудочно-кишечном тракте, поэтому достаточно долго преимущественным способом введения оставался парентеральный. При внутримышечном и подкожном введении биодоступность составляет 80%, максимальная концентрация в крови достигается в среднем через 3,8 ч. Установлено, что при внутривенном капельном введении 6–9 млн МЕ ИФНα2b (реаферон) в течение 1 ч ИФН определялся в сыворотке крови уже через 30 мин от начала введения .Через 2,5 ч титры ИФН снижались на 50%, спустя 4 ч определялись только его следовые количества. Известно, что почки выводят ИФН по крайней мере со скоростью 2% в минуту, таким образом, очищение плазменного пула происходит меньше чем через час. Введение больших доз ИФН, помогающих преодолеть эти быстрые потери, ограничено токсическим порогом действия препарата на ЦНС, а также подавлением системы иммунитета. При внутримышечном введении ИФН поступает в системный кровоток через капилляры, уровень ИФН в плазме снижается медленнее по сравнению с внутривенным введением. При внутримышечном введении повышенное содержание ИФН в плазме регистрируется в период от 1 до 6 ч, снижение до исходного уровня определяется через 12 ч после введения препарата.
В экспериментальном изучении фармакокинетических параметров рекомбинантного ИФНα2b с антиоксидантами (витамины Е и С) (ВИФЕРОН) у новорожденных и половозрелых кроликов было показано, что введение ИФН в виде суппозиториев в прямую кишку приводит не только к высокому содержанию препарата в плазме крови, но и более длительной циркуляции высоких концентраций ИФН, чем при его введении через катетер (табл. 2) .
Расчет фармакокинетических параметров показал, что относительная биодоступность при введении препарата ВИФЕРОН ректально в виде суппозиториев в дозе 150 000 МЕ новорожденным животным составляет 1,5 по сравнению с введением той же дозы ИФН животным через катетер. У половозрелых кроликов относительная биодоступность при введении препарата ВИФЕРОН ректально в дозе 150 000 МЕ составляет 1,23 по сравнению с введением той же дозы животным через катетер (табл. 3).
Таким образом, сравнительный анализ основных фармакокинетических параметров рекомбинантного ИФНα2b с антиоксидантами, характеризующий биоэффективность препарата, показал, что его применение в виде ректальных суппозиториев имеет значительное преимущество перед введением с помощью катетера.
Интересные данные были получены при изучении терапевтической эффективности лимфобластного ИФНα в виде ректальных суппозиториев у 28 больных хроническим вирусным гепатитом С. Авторами было показано, что назначение низких доз (1000 МЕ) ИФН в течение 4 недель способствовало снижению уровня РНК вируса гепатита С с 5,65±0,18 до 5,17±0,7,65 Log МЕ/мл (р=0,01), повышению активности 2’-5’олигоаденилат синтетазы и достоверному снижению соотношения CD4/CD8, что позволило сделать вывод, что ректальный способ введения ИФН является безопасным и эффективным и может рассматриваться в качестве альтернативы внутривенному способу .
| Время после введения препарата | Новорожденные кролики | Взрослые кролики | ||
| Концентрация ИФН, МЕ/мл | ||||
| введение в виде суппозиториев | введение через катетер | введение в виде суппозиториев | введение через катетер | |
| 30 мин | 19,2±3,2 | 16,0±4,4 | 28,8±3,2 | 25,6±3,9 |
| 1ч | 22,4±3,8 | 16,0±4,4 | 25,6±3,9 | 25,6±3,9 |
| 2ч | 19,2±3,2 | 16,0±4,4 | 25,6±3,9 | 17,6±3,9 |
| 3ч | 19,2±3,2 | 16,0±4,4 | 22,4±3,9 | 14,8±5,0 |
| 4ч | 19,2±3,2 | 12,8±2,0 | 14,4±1,6 | 15,2±4,8 |
| 5ч | 20,8±4,8 | 10,4±2,4 | 12,8±2,0 | 12,0±2,5 |
| 6ч | 10,4±2,4 | 1,8±0,58 | 9,0±3,0 | 3,8±1,3 |
| 7ч | 10,4±2, | 1,8±0,24 | 4,8±0,8 | 3,8±1,3 |
| 8ч | 1,6±0,24 | 1,6±0,24 | 1,6±0,24 | 1,6±0,24 |
| Время после введения препарата | Новорожденные кролики | Взрослые кролики | |||
| введение в виде суппозиториев | введение через катетер | введение в виде суппозиториев | введение через катетер | ||
| Концентрация-время | AUC МЕ, мин/мл | 7,58±0,34 | 4,96±0,24 | 7,4±0,45 | 5,97±0,69 |
| Произведение времени на концентрацию-время | AUMCМЕ, мин2/мл | 1,58±0,12 | 0,865±0,044 | 1,3±0,09 | 0,997±0,15 |
| Клиренс | Cl, мл/мин | 208,6±10 | 175,9±10 | 175,0±4,96 | 163,8±6,97 |
| Период полувыведения | T1/2, мин | 19,9±0,9 | 30,6±1,6 | 20,6±1,4 | 26,7±3,4 |
| Максимальная концентрация | Cmax | 32,0±3,2 | 25,6±3,9 | 32,0±3,2 | 32,0±3,2 |
| Время достижения максимальной концентрации | Tmax | 162,0±52 | 96,0±35 | 36,6±6 | 42,0±7,3 |
| Относительная биодоступность | f | 1,5 | 1,23 |
Криданимод
Данная химическая субстанция также достаточно популярна на территории стран СНГ и Дальнего Востока. Она является производным акридина, химическое название — 10-карбоксиметил-9-акриданон. Перед непосредственным обсуждением свойств криданимода необходима небольшая ремарка. Исторически сложилось так, что существует несколько систем классификации органических соединений, вследствие чего иногда одной и той же субстанции могут присваиваться различные названия. И, если использовать химическое название, а не международное непатентованное наименование (МНН), это может вводить в заблуждение как специалистов здравоохранения, так и пациентов. Оксодигидроакридинилацетат натрия и кислота акридонуксусная, на первый взгляд, кажутся разными действующими веществами. Однако, если обратиться к международным ресурсам, предоставляющим информацию касательно номенклатуры химических субстанций, можно увидеть, что упомянутые названия — синонимы. Это может быть связано с тем, что поскольку катион натрия является сильным основанием, а акридонуксусная кислота — слабым электролитом, то в водном растворе наступает динамическое равновесие, и протоны водорода замещают ион натрия.
Помимо этого, в некоторых источниках кислота акридонуксусная фигурирует под другим названием — меглюмина акридонацетат (именно под таким названием эта субстанция включена в Перечень жизненно важных и необходимых лекарственных препаратов Российской службой по федеральному надзору в сфере здравоохранения).
Данный пример свидетельствует о том, что необходимо использовать унифицированную систему наименования лекарственных средств, коей является обозначение действующих веществ с помощью МНН. Вследствие приведенных противоречий специалисты здравоохранения и пациенты могут испытывать трудности, связанные с поиском интересующей их информации о свойствах препаратов.
Необходимо отметить, что в настоящее время в США криданимод находится на стадии доклинических исследований, в ходе которых изучается его роль в комплексной терапии гормонрезистентного рака эндометрия. Интерес ученых к молекуле связан с тем, что ранее было продемонстрировано свойство криданимода увеличивать экспрессию рецепторов прогестеронов в эндометрии крыс.
Примечательным является тот факт, что на достоверных международных информационных ресурсах нет данных о проведении клинических исследований в США и странах ЕС таких субстанций, как кагоцел, умифеновир, оксодигидроакридинилацетат натрия, кислота акридонуксусная (меглюмина акридонацетат).
Эти химические соединения являются действующими веществами препаратов, зарегистрированных в Украине, которые принимают для профилактики и лечения ОРВИ, гриппа и других вирусных инфекций. Их применение ограничивается странами СНГ и некоторыми государствами Дальнего Востока.
С чем это может быть связано, учитывая отсутствие достоверной информации с международных источников относительно профиля безопасности индукторов интерферона?
Понимая потенциальную опасность для здоровья, к этому вопросу следует подходить максимально серьезно. Ведь реальное влияние веществ, воздействующих на регуляцию сигнальных путей клетки, на здоровье может быть выявлено через десятки лет. Предположить, что производители этих препаратов знают о потенциальном риске, но все равно продолжают их выпускать, невозможно. Или мы имеем дело со случаем крайнего цинизма?
Галина Галковская, по материалам http://www.ncbi.nlm.nih.gov; pubchem.ncbi.nlm.nih.gov; iai.asm.org; http://www.plosone.org; http://www.dtic.mil; aac.asm.org; chem.sis.nlm.nih.gov; ebm.sagepub.com; http://www.depts.ttu.edu; http://www.reference.md; http://www.nlm.nih.gov; vir.sgmjournals.org; meetinglibrary.asco.org; http://www.fda.gov; http://www.jbmb.or.kr
Интерферон лейкоцитарный человеческий
Это лекарство, представляющее собой комплекс белков,
получают из донорской крови. Доступно в виде таблеток или пористого порошка. Не
содержит антитела к вирусам иммунодефицита человека и гепатита группы С. Имеет
широкий спектр антивирусного действия. Применяется в одинаковой дозировке для
лечения детей и взрослых. Если вводится через дыхательные пути, не вызывает
каких-либо побочных эффектов. Категорически запрещено инъекционное использование
лекарственного средства.
Когда показан и противопоказан?
Интерферон
лейкоцитарный применяется с целью проведения профилактики, лечения гриппа, других
респираторных инфекций вирусной природы (ОРВИ). Для терапии необходимо
использовать лекарство на ранних стадиях развития болезни, когда наблюдаются
первые клинические проявления. Раннее назначение повышает терапевтическую
эффективность. Если вводится через дыхательные пути, противопоказания
отсутствуют.
Особенности применения
Препарат
растворяется в 2 миллилитрах стерильной или кипячённой воды, имеющей комнатную
температуру. Его можно закапывать, распылять или вводить ингаляционным путём в
носовую полость. Для распыления лекарственного средства используется любой
современный медицинский распылитель. Ингаляции или распыления делаются дважды в
день с перерывом более 6 часов. Если закапывать, то по пять капель в каждую
ноздрю 5-7 раз в день на протяжении двух-трёх суток. Побочные эффекты
отсутствуют
Использовать с предельной осторожностью нужно пациентам, у которых
повышенная чувствительность (аллергия) на антибактериальные препараты или куриные
белки. Перед применением обязательно проконсультироваться с лечащим врачом
Виды искусственных интерферонов
В зависимости от способа получения противовирусного
лекарства, интерферон
может быть следующих видов:
-
Лейкоцитарный.
Кровь донора — основной источник для получения этой разновидности интерферона.
Для усиления выработки необходимых белковых веществ проводят стимуляцию клеток
иммунной системы, используя непатогенные вирусы. Они не способны спровоцировать
развитие болезни, но воспринимаются организмом как «потенциальная
опасность», требующая устранения. Получив нужные вещества, препарат очищается,
концентрируется. Обладает сильным потенциалом терапевтического действия, но высок
риск возникновения побочных реакций, поскольку содержит все типы это защитного
белка. -
Лимфобластоидный.
Для его получения используют лимфобластные клетки, на которые воздействуют
специальными частицами, вызывающими стимуляцию иммунного ответа. Эти противовирусные препараты имеют
несколько видов интерферонов, но в меньшем соотношении, чем предыдущие
лекарства. Поэтому не особо часто провоцируют побочные реакции при инъекциях. -
Рекомбинатный.
Как правило, добывают из культур бактериальных клеток, в которые вводят часть
гена человека. Интерферон,
получаемый подобным способом, имеет некоторые отличия, по сравнению с
«природным» человеческим. Для него характерна противовирусная
активность, но он слабо стимулируют иммунитет. -
Пегилированный.
Является рекомбинантной белковой молекулой, которая соединена с
полиэтиленгликолем, что позволяет увеличить продолжительность действия
антивирусного лекарства.
Показания к применению интерферона
ИнтерферонывирусовИнтерферонпротивовирусноерассеянного склерозаАльфа-интерферон показан к использованию в следующих случаях:
- клещевой энцефалит;
- хронический вирусный гепатит В и С;
- саркома Капоши (злокачественное заболевание, связанное с ВИЧ);
- кандидоз;
- злокачественные новообразования кожи (в том числе меланома);
- злокачественные заболевания крови (волосатоклеточный лейкоз, хронический миелоидный лейкоз);
- злокачественные новообразования почек;
- микоз;
- профилактика и лечение гриппа и ОРВИ (острых респираторных вирусных инфекций);
- для профилактической иммунотерапии.
Бета-интерферон применяется при следующих заболеваниях:
- герпетическая инфекция;
- опоясывающий лишай;
- вирусные бородавки (папилломавирус человека);
- хронический гепатит В и С;
- рассеянный склероз;
- злокачественные поражения молочных желез, матки, крови, кожи.
Интерферон при вирусном гепатите (В, С)
более 6 месяцевциррозу печениракурибавирин, ламивудинальфаферон, пегасис, пегинтронвоспроизводствапечениАЛТ, АСТ
Использование интерферона при лечении хронических вирусных гепатитов преследует следующие цели:
- уменьшение воспроизводства вируса;
- уменьшение воспаления;
- предотвращение перехода гепатита в цирроз или в карциному.
3 миллиона МЕ 3 раза в неделю10 миллионов МЕ ежедневнодостижение полного выздоровления
Интерферон при герпесе
ветрянкипузырьки на коже и слизистых оболочках, наполненные серозной жидкостью20000 МЕ/млацикловирлидокаинзудне всасывается в кровь и не дает побочных эффектов
Интерферон при конъюнктивите, кератите и других заболеваниях глаза
Заболевания глазслепотаконъюнктивит, кератитофтальмологиглазные каплиофтальмоферонОфтальмоферон обладает следующими свойствами:
- противовирусным (основное действие интерферона);
- антибактериальным (содержит борную кислоту);
- противоаллергическим;
- противоотечным;
- смазывание глазного яблока (полимерная основа имитирует действие искусственной слезы).
Интерферон при папилломах
Для лечения папиллом применяют следующие препараты интерферона:
- Виферон. Используется в виде геля, мази (местно) и свечей (системно).
- Интрон. Используется системно в виде внутримышечных инъекций.
- Роферон. Вводится подкожно по 1 – 3 миллионов МЕ 3 раза в неделю. Длительность лечения составляет 1 – 2 месяца.
- Вэллферон. Вводится подкожно по 5 миллионов МЕ 3 раза в неделю.
Интерферон при рассеянном склерозе
головного мозганаправленная не на симптомы, а на причину возникновения заболеванияребиф, бетаферонот 6 месяцев до 1 года
https://youtube.com/watch?v=I3tBWpnpB5w
Интерферон при полицитемии
Истинная полицитемия (болезнь Вакеза)цитостатикициклофосфандля уменьшения вязкости крови — гематокритатромбоцитовэритроцитовдлится более 6 месяцевдостигнута полная ремиссия
Интерферон при бронхите
Бронхитчто очень сложно выполнить
При лечении бронхита используются следующие группы препаратов:
- противовоспалительные средства;
- отхаркивающие средства;
- оральные антисептики;
- в тяжелых случаях – антибиотики.
Интерферон при токсоплазмозе
Токсоплазмозбактериитоксоплазмавысокой температуройголовной больюрвотойсудорогамиантителаДля лечения токсоплазмоза используются следующие антибактериальные препараты:
- сульфадиазин;
- клиндамицин;
- спирамицин;
- азитромицин;
- левамизол.
Способы получения интерферонов, классификация
Для получения интерферона применяются методы:
- инфицирования человеческих факторов защиты крови (лимфоцитов, лейкоцитов) определенными безопасными штаммами вирусов. Затем выделяемый клетками интерферон проходит технологические методы обработки и превращается в лекарственную форму;
- генного конструирования (рекомбинантный) – искусственное выращивание бактерий (чаще всего кишечных палочек), с имеющимся геном интерферона в ДНК. Запатентованное название интерферона, выпускаемого по этой методике, – «Реаферон».
Обратите внимание: производство «Реаферона» намного дешевле лейкоцитарного интерферона, а эффективность может быть большей. Рекомбинатный интерферон применяется при лечении не только вирусных заболеваний.
Исходя из полученной информации, выделим основные виды интерферона:
- Лимфобластоидные ИТФ – полученные из естественных материалов.
- Рекомбинантные ИТФ – синтетические аналоги человеческих итерферонов.
- Пегилированные ИТФ – синтезируются совместно с полиэтиленгликолем, позволяющим интерферонам действовать дольше обычного срока. Они обладают более сильным лечебным действием.
Клинико-фармакологические аспекты преимуществ комбинации ИФН с антиоксидантами. Фармакокинетическое взаимодействие
В исследовании П.А. Джумиго проведено изучение накопления ИФН у здоровых добровольцев, которые были разделены на 3 группы в зависимости от способа введения препарата: в 1-й группе ИФНα2b (реаферон) вводился ректально в виде клизмы однократно в дозе 1 000 000 МЕ; во 2-й группе ректальное введение препарата ИФНα2b (реаферон) сочеталось с одновременным внутримышечным введением 2 мл 30% масляного раствора α-токоферола ацетата; в 3-й – ректальное введение препарата ИФНα2b (реаферон) сочеталось с одновременным внутримышечным введением 2 мл 30% масляного раствора α-токоферола ацетата и 2 мл 10% раствора аскорбиновой кислоты.
Во всех группах проводилось определение концентрации ИФН в сыворотке крови перед введением и через 1, 2, 4, 8, 12 и 24 ч после его введения.
Исследование фоновых уровней ИФН в крови перед назначением ИФНα2b в 1-й группе показало, что высокие титры ИФН выявляются уже через 1 ч после его введения, причем максимальные титры ИФН приходились на промежуток времени, соответствующий 1 и 2 ч после его введения. Через 4 ч концентрация препарата снижалась в 2–4 раза. У одного добровольца этой группы концентрация ИФН в плазме крови возвращалась к фоновым значениям спустя 8 ч. У остальных волонтеров начальные титры ИФН не отличались от таковых в порциях плазмы крови, полученных через 12 ч после введения ИФНα2b (реаферона).
Сочетание ИФНα2b (реаферона) с внутримышечным введением витамина Е (α-токоферола ацетата) изменяло динамику накопления ИФН в сыворотке крови добровольцев 2-й группы. Через 1 ч после введения препаратов наблюдалось повышение уровня ИФН по сравнению с исходными значениями в 4–8 раз, но максимальные уровни сывороточного ИФН были отмечены в порциях сывороток, полученных через 4 ч после введения рекомбинантного ИФН. Через 8 ч титры ИФН у большинства добровольцев оставались более высокими, чем фоновые. Через 12 ч у добровольцев уровень ИФН в плазме крови продолжал снижаться, а у одного волонтера наметилась тенденция к его повышению.
В последней группе, где применение ИФН α2b сочеталось с введением двух антиоксидантов (витамин Е и С), повышение уровня сывороточного ИФН регистрировалось через 1 ч после ректального введения. Наиболее высокие показатели у доноров были отмечены через 2 ч после введения комбинации препаратов. К 8 ч происходило снижение титров сывороточного ИФН, но после этого срока до 12 ч сывороточный ИФН держался на высоком уровне и к 24 ч уровни его в 4–8 раз превышали первоначальные фоновые значения сывороточного ИФН.
Сравнение фармакокинетики ректального введения ИФНα2b (реаферона), как отдельно, так и в комплексе с антиоксидантами, выявило ощутимые различия. При ректальном введении препарата удается достичь быстрых высоких концентраций ИФН в сыворотке испытуемых, тогда как сочетание с антиоксидантами ведет к постепенному повышению титров ИФН. Так, использование одного ИФНα2b дает повышение титров ИФН через 1 ч после введения, а комбинированное применение с антиоксидантами демонстрирует максимальные показатели ко 2–4 ч. Добавление одного из антиоксидантов приводит к быстрой элиминации экзогенного ИФН – возвращение к фоновым показателям наблюдается через 8–12 ч, в то время как сочетание двух антиоксидантов ведет к более длительной циркуляции экзогенно введенного ИФНα2b в токе крови и сохранению высоких показателей ИФН через 12 ч наблюдения.
Таким образом, было показано, что ректальное применение ИФНα2b дает возможность достичь высоких уровней сывороточного ИФН при относительно небольших дозах препарата, что повышает безопасность его использования и позволяет избежать нежелательных явлений, которые наблюдаются при введении больших доз ИФН (головная боль, артралгии, лейкопения). Применение антиоксидантов также препятствует быстрой элиминации препарата из крови – в течение 12 ч и более.
Какие препараты интерферона лучше выбрать
На этикетке любого лекарства, сделанного на основе интерферона, можно прочесть, скажем, такую малопонятную фразу: «человеческий лейкоцитарный γ-интерферон». На другом лекарстве надпись уже будет гласить, что это «рекомбинантный α-интерферон». Или «рекомбинантный γ-интерферон» и «генно-инженерный α-интерферон». Что же это все значит?
Что такое, например, α (альфа), β (бета)и γ (гамма)? Это молекулярный вес тех самых молекул интерферона, которые были использованы при изготовлении того или иного лекарства. На практике это означает всего-навсего, с какой скоростью эти молекулы будут выброшены вон из организма. Медленнее всех выводится α, чуть побыстрее β, ну а γ вовсе вылетает со свистом, едва попав в организм. Гамма-интерфероны назначают часто, альфа-интерфероны — редко.
Гораздо интереснее, что значат таинственные слова «генно-инженерный», «рекомбинантный» и «человеческий лейкоцитарный». Это — своеобразный отчет производителя, где же он взял этот самый интерферон, прежде чем продать его вам.
«Человеческий лейкоцитарный интерферон» означает, что интерферон получен из донорской крови — так, как его получали еще в 1970-х годах. Разумеется, доноров — даже тех, чья кровь идет на сугубо технические нужды (например, на получение интерферона) самым тщательным образом проверяют, но даже в самом частом сите все равно случаются дырки. Если вы боитесь СПИДа, сифилиса или гепатита, лучше выбрать другой интерферон — генно-инженерный или рекомбинантный, полученные вовсе не из донорской крови. А из чего тогда?
Источники генно-инженерного интерферона — микроорганизмы, которые тысячелетиями живут бок о бок с человеком. Например, кишечная палочка. Согласитесь, симбиоз этот далеко не всегда приятен — по крайней мере, нам с вами. Вот специалисты по биотехнологиям и заставили кишечную палочку немножко отработать за все те художества, которые она творила.
Как? Да очень просто. Взяли ген из человеческой клетки, ответственный за производство интерферона, подсадили его кишечной палочке и заставили последнюю вырабатывать интерферон в промышленных количествах. Получилось, во-первых, дешевле, чем выделять интерферон из донорской крови, а во-вторых, гораздо безопаснее. У кишечной палочки хоть гепатита не бывает. Правда, в итоге получилось, что эта самая кишечная палочка оказалась генно-модифицированным организмом, сокращенно — ГМО.
Что страшнее — риск заразиться гепатитом из-за плохо очищенного донорского интерферона или риск от употребления загадочного продукта генной инженерии? Наверное, все-таки первое. Генно-модифицированные кишечные палочки в готовые препараты интерферона все же не попадают.

Преимущество индукторов эндогенного протеина
Существует два способа повышения иммунитета интерфероном. Данное соединение можно вводить экзогенно или непосредственно в организм. Другой путь подразумевает эндогенную интерферонизацию с введением веществ, стимулирующих выработку собственного интерферона. Такой белок не проявляет антигенности, чего нельзя сказать о рекомбинантном интерфероне. Длительное введение готового протеина в виде препаратов приводит к развитию нежелательных реакций.
Индукторы эндогенного интерферона при изучении их эффективности показали фармакологическую активность в широком спектре инфекций. Было установлено их бифункциональное свойство, характеризующееся антивирусным влиянием и выраженным иммуномодулирующим эффектом.
Действие индукторов интерферона приводит к синтезу белков, которые по своей активности похожи на готовые защитные протеины. Такой процесс считается сбалансированным, его контролируют механизмы, которые надежно защищают организм от избыточного образования данных соединений.
При однократном применении препаратов, индуцирующих интерферон, происходит довольно длительная циркуляция защитного белка в нужной терапевтической дозе. Для получения такой дозировки при назначении экзогенного протеина его следует многократно вводить в больших объемах. Такое лечение считается более дорогостоящим.
Применение Интерферона

Интерферон прост для применения. Лечение должно проводиться только под контролем специалиста, который уже использовал средство для терапии. Наиболее применимые лекарственные формы: инъекционный раствор, глазные капли, пленки, назальные капли и спрей. Самый распространённый способ использования – инъекционное введение препарата.
Остальные формы лекарства имеют строго установленную дозировку действующего вещества. Обычно Интерферон поставляют в виде порошка, находящегося в стеклянных ампулах. Лекарство разводится водой для инъекций.
Если оно вводится внутримышечно, используется 1 мл воды для инъекций, при субконъюнктивальном и местном введении – 5 мл. Раствор должен быть прозрачным. Когда раствор будет готов, следует сразу использовать его.
Препарат могут вводить в область плеч, в боковую и переднюю поверхность бедра. Очень часто при введении лекарства используют большую ягодичную мышцу. В это место иглу вводят не более, чем на 3 см. Иногда препарат вкалывают в другие области, такие как подлопаточная область, боковая стенка живота. Раствор должен вводиться так, чтобы игла проникала внутрь на 15 мм.
Практикуют и субконъюнктивальную инъекцию. Она выполняется в поверхностную слизистую оболочку глаза.
Для лечения

Для лечения применяется спрей, который впрыскивается в вертикальном положении
Важно помнить, что каждый член семьи должен приобрести свой флакон, чтобы не распространить инфекцию через дозатор. Если такой возможности нет, его следует обрабатывать раствором спирта, концентрация которого должна превышать 60%
Следует капать капли или использовать спрей 5-6 раз в день вместе с мефлохином, который рекомендуют принимать по 500 мг в первый и второй день, то есть два раза по 250 мг. Если есть противопоказания к использованию мефлохина и гидроксихлорохина, то следует применять тот же вид интерферона с такой же дозировкой, но вместе с умифеновиром, который принимают по 200 мг 4 раза в день в течение 5 дней.
Что касается рекомбинантного Интерферона бета-1б, его вводят в организм с помощью инъекций. А именно по 0,25 мг в течение двух недель. Это равно 7-ми инъекциям данного препарата.
Если человек обнаружил первые признаки заболевания, нужно интраназально использовать гамма человеческий рекомбинантный подвид препарата, принимая две капли после промывания носовых полостей пять раз в сутки. Терапия будет длиться 5-7 суток.
Для профилактики

Если у человека был контакт с больным, то следует использовать Интерферон для профилактики. Минздрав рекомендует применять капли или спрей интерферона альфа 2b строго в каждый носовой проход два раза в день 14 дней. Если же контакт был однократным, то нужно закапать интерферон гамма человеческий один раз в каждый носовой проход.
В свою очередь, гамма человеческий рекомбинантный (он противопоказан беременным и детям младше семи лет) нужно закапывать 2 капли интраназально за полчаса до первого приема пищи в течение десяти дней. Если необходимо, курс повторяют. А если взаимодействие было единичным, закапывают один раз.