Штамм бактерий pseudomonas putida, используемый для очистки почв, грунтовых и поверхностных вод от тринитротолуола
Содержание:
- Иммунитет
- Acinetobacter spp.
- Основные бактериологические характеристики[править | править код]
- Группы в Pseudomonas senso stricto
- De Wikipedia, la enciclopedia libre
- Общие характеристики
- Биологическое регулирование численности организмов
- Этиология и распространение заболевания
- Лечение
- Metabolism
- 4 ответа
- References
- Current Research
Иммунитет
В процессе заболевания в сыворотке крови больных образуются типоспецифические антибактериальные и антитоксические антитела, роль которых в защите от повторных заболеваний мало изучена.
ССЫЛКИ ПО ТЕМЕ
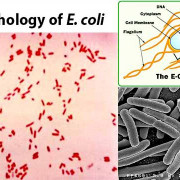
Что такое цитоплазма
Статьи раздела «Синегнойная инфекция»
- Все о синегнойной палочке
Самое популярное
- Все о грибке стопы: симптомы и эффективное лечение современными препаратами
- Грибок кожи головы: как распознать и лечить
- Симптомы и лечение грибка ногтей на руках (онихомикоза)
- Польза и вред кишечной палочки
- Как лечить дисбактериоз и восстановить микрофлору
Статьи раздела «Синегнойная инфекция»
- Все о синегнойной палочке
О микробах и болезнях 2020
Acinetobacter spp.
Занимают второе после P. aeruginosa место по клиническому значению среди неферментирующих микроорганизмов. Межвидовая дифференцировка (A. baumannii, A. lwoffii, A. haemoliticus и др.) внутри рода может быть затруднена
Ацинетобактеры широко распространены в природе и, что особенно важно, в стационарах, особенно хирургического профиля, в отделениях реанимации и интенсивной терапии. Микроорганизмы сохраняют жизнеспособность во многих растворах, на сухих и влажных поверхностях оборудования и достаточно быстро колонизуют кожные покровы и слизистые оболочки пациентов.
Для здоровых людей ацинетобактеры практически непатогенны, однако в отделениях интенсивной терапии и реанимации могут способствовать развитию тяжелых инфекций
Наиболее часто микроорганизмы вызывают респиратор-ассоциированные пневмонии, доказана их роль и в этиологии госпитальных инфекций другой локализации (инфекции мочевыводящих путей, менингиты, эндокардиты, остеомиелиты, перитониты и др.). Описаны вспышки госпитальных инфекций, вызванных ацинетобактерами.
При выделении ацинетобактеров требуется тщательная оценка их клинической значимости и дифференцировка инфекции от колонизации.
Ацинетобактеры характеризуются высоким уровнем природной чувствительности к большинству антибиотиков, однако их характерной особенностью является быстрое формирование приобретенной устойчивости к антибактериальным препаратам многих групп. Госпитальные штаммы ацинетобактеров, как правило, полирезистентны.
Основные бактериологические характеристики[править | править код]
У представителей вида чрезвычайно гибкий метаболизм. Они могут обитать в воде и почве. Являются облигатными аэробами, но некоторые штаммы способны использовать нитраты вместо кислорода в качестве конечного акцептора в процессе клеточного дыхания. Оптимальная температура для роста P. fluorescens составляет 25—30 °C. Даёт положительные результаты в тесте на оксидазуruen. Также является несахаролитической бактерией.
Бактерией P. fluorescens и другими подобными псевдомонадами вырабатываются термостабильные липазы и протеазы. Эти ферменты вызывают порчу молока, придают ему горечь, разлагая казеины и в дальнейшем обуславливают появление в нём нитей полисахаридов за счёт выработки слизи и коагуляции белков.
Биологический распадправить | править код
В P. fluorescens обнаружен фермент 4-гидроксиацетофенон-монооксигеназаruen, который преобразует Piceolruen в 4-гидроксифенилуксусную кислотуruen.
Группы в Pseudomonas senso stricto
На основе анализа мультилокусной последовательности было предложено Pseudomonas Он будет разделен на пять групп:
группа P. fluorescensэто очень разнообразно, и виды — сапрофиты, присутствующие в почве, воде и поверхности растений. Многие виды способствуют росту растений.
группа P. syringae: состоит в основном из видов, которые фитопатогены. Распознано более пятидесяти патоваров (штаммы бактерий с разной степенью патогенности).
группа П. Путида: виды этой группы встречаются в почве, ризосфере различных растений и в воде. Они обладают высокой способностью к разложению веществ.
группа P stutzeriэти бактерии имеют большое значение в круговороте питательных веществ и обладают высоким генетическим разнообразием.
группа P aeruginosa: эта группа представляет виды, которые занимают различные места обитания, в том числе патогенные.
Тем не менее, в более недавнем молекулярном исследовании предлагается разделить пол на тринадцать групп, состоящих из двух или более шестидесяти видов..
Самая большая группа — это P. Fluorescens, который включает типовые виды, которые широко используются в программах биоремедиации. Другой вид интереса в этой группе P. mandelii, которая растет в Антарктиде и показала свою высокую устойчивость к антибиотикам.
De Wikipedia, la enciclopedia libre
| Pseudomonas fluorescens | |
|---|---|
| Taxonomía | |
| Dominio: | Bacteria |
| Filo: | Proteobacteria |
| Clase: | Gammaproteobacteria |
| Orden: | Pseudomonadales |
| Familia: | Pseudomonadaceae |
| Género: | Pseudomonas |
| Especie: | P. fluorescensMigula, 1895 |
Pseudomonas fluorescens es un bacilo Gram-negativo, recto o ligeramente curvado pero no vibrioide, es saprofito, (todo lo que ingiere pasa a través de la pared de su citoplasma). Se puede encontrar en suelo y agua.
Es incapaz de formar esporas y crece aeróbicamente. La temperatura óptima para su funcionamiento es de 25 a 30 °C, aunque puede crecer desde los 5 hasta los 42 °C aproximadamente. No crece bajo condiciones ácidas (pH ≤ 4.5) y necesita preferentemente pH neutro. Tiene movimiento activo en líquido por sus flagelos polares (más de 1). Su pigmento fluorescente (fluoresceína) la hace reaccionar frente a la luz ultravioleta, aunque recién cultivada o después de varios cultivos de laboratorio, puede ser que no reaccione.
Las Pseudomonas pueden crecer en un medio mineral con iones de amonio o nitrato y un solo compuesto orgánico que funciona como única fuente de carbono y energía. La ganancia energética es obtenida por respiración aeróbica, no por fermentación y su crecimiento es rápido.
Abundan en la superficie de las raíces, ya que son versátiles en su metabolismo y pueden utilizar varios sustratos producidos por las mismas, pero no establecen una relación simbiótica con la planta.
Una de las características de la Pseudomonas fluorescens es su alta capacidad de solubilización del fósforo y la realizan por dos vías: la primera es la producción de ácidos orgánicos (ácido cítrico, ácido oxálico, ácido glucónico) que actúan sobre el pH del suelo favoreciendo la solubilización del fósforo inorgánico y liberando el fosfato a la solución del suelo. La otra vía de acción es a través de las fosfatasas que son enzimas hidrolasas (Monoesterasas y Diesterasas Fosfóricas) que actúan sobre las uniones ésteres liberando los grupos fosfatos de la materia orgánica a la solución del suelo. Ambas vías generan una mayor cantidad de fosfato para ser absorbido por las raíces de las plantas.
Otro aspecto destacable es la posibilidad de que las Pseudomonas fluorescens posean la virtud de producir sustancias estimuladoras del crecimiento, ya que las Pseudomonas en general pertenecen a un grupo llamado “estimuladores del crecimiento vegetal (MECV)” que poseen la propiedad de producir estas sustancias, cuyas principales ventajas son las de estimular la germinación de las semillas, acelerar el crecimiento de las plantas especialmente en sus primeros estadios, inducir la iniciación radicular e incrementar la formación de raíces y pelos radiculares. Las principales sustancias estimuladoras producidas son de tipo hormonal como auxinas, giberelinas y citoquininas, pero también producen sustancias de otro tipo como aminoácidos y promotores específicos del crecimiento. Estos efectos se dan siempre que sea adecuada la concentración de organismos en el sistema radicular y en el suelo haya suficiente cantidad de materia orgánica.
Por último, una propiedad complementaria de la Pseudomonas fluorescens es la de producir ciertas sustancias -antibióticos y sideróforos- que actúan limitando el crecimiento y desarrollo de los patógenos fúngicos que pueden afectar al cultivo.
- Datos: Q135292
- Multimedia:
- Especies: Pseudomonas fluorescens
Общие характеристики
распределение
Из-за его большой способности расти в разнообразных средах, род имеет повсеместное экологическое и географическое распространение. Они были найдены в наземных и водных средах. Они хемотрофны и легко выращиваются в питательных питательных средах на агаре.
температура
Его идеальный температурный диапазон составляет от 25 до 30 ° C. Тем не менее, были найдены виды, растущие при температуре ниже нуля, а другие выше 50 ° C.
болезни
Среди видов, составляющих род, есть такие, которые вызывают болезни у животных и людей. Кроме того, многие виды являются патогенными растениями, вызывающими так называемую мягкую гниль..
приложений
Другие виды могут быть очень полезными, поскольку было доказано, что они стимулируют рост растений и могут применяться в качестве удобрений. Они также могут разлагать ксенобиотические соединения (которые не входят в состав живых организмов)..
Некоторые из ксенобиотиков, которые могут разлагаться, включают ароматические углеводороды, хлораты и нитраты. Эти свойства делают некоторые виды очень полезными в программах биоремедиации..
Окрашивание и дыхание
Виды Pseudomonas Они грамотрицательные. Они в основном аэробные, поэтому кислород является конечным рецептором электронов в дыхании.
Некоторые виды могут использовать нитраты в качестве альтернативных акцепторов электронов в анаэробных условиях. В этом случае бактерии восстанавливают нитраты до молекулярного азота..
идентификация
Все виды Pseudomonas Они каталазы положительные. Это фермент, который расщепляет перекись водорода на кислород и воду. Большинство аэробных бактерий производят этот фермент.
В группе есть положительные и отрицательные виды оксидаз. Присутствие этого фермента считается полезным при идентификации грамотрицательных бактерий.
Большинство видов накапливают полисахарид глюкозы в качестве резервного вещества. Однако некоторые группы могут иметь полигидроксибутират (ПГБ), который является полимерным продуктом ассимиляции углерода..
Биологическое регулирование численности организмов
Некоторые штаммы P. fluorescens (например, CHA0 или Pf-5) проявляют способность биоконтроля, защищая корни некоторых видов растений от паразитных грибков, таких как фузарий или питиозная корневая гнильruen, а также от некоторых растительноядных нематод.
Не совсем ясно, как Ф. псевдомонада проявляет свойства, активирующие рост растений. Есть несколько версий на этот счёт:
- бактерии могут провоцировать системную сопротивляемость растения-хозяина, для улучшения устойчивости к атакам истинных патогенов;
- бактерии могут вытеснять другие (патогенные) почвенные микроорганизмы, например, сидерофорыruen, дав растению конкурентное преимущество для захвата железа;
- бактерии могут вырабатывать соединения, антагонистические для других почвенных микроорганизмов, например такие, как синильная кислота или антибиотики на основе феназина;
Если быть точнее, то определённые изоляты Ф. псевдомонады производят вторичные метаболиты 2,4-диацетилфлороглюцинаruen (далее 2,4-ДАФГ), состав которых, как полагают, ответственен за анти-фитопатогенность и за свойства биоконтроля в этих штаммах. Генный кластер флороглюцина отвечает за генный фактор 2,4-ДАФГ в аспекте биосинтеза, регуляции, оттока и распада.
Восемь генов флороглюцина (HGFACBDE) ruen в этом кластере и организационно закреплены за производством 2,4-ДАФГ штаммов Ф. псевдомонад. Из этих генов, ген D отвечает за поликетидсинтазы типа III, предоставляя ключевой биосинтетический фактор для производства 2,4-ДАФГ. Ген D демонстрирует сходство с халконсинтазойruen и, теоретически, происходит из горизонтального переноса генов. Однако, филогенетический и анализы показали, что весь флороглюциновый кластер генов, это потомок Ф. псевдомонады, и много штаммов потеряли продуктивность, что имеет место в различных геномных областях среди штаммов.
Существуют экспериментальные свидетельства в поддержку этих теорий для определённых условий. Обзор данной темы описан Хаасом и Дефаго.
Несколько штаммов Ф. псевдомонады, таких как Pf-5 и JL3985, развили естественную устойчивость к ампициллину и стрептомицину.
Эти антибиотики регулярно используются в биологическом исследовании в качестве инструмента селективного давления, чтобы вызвать транскрипцию и трансляцию плазмиды.
Штамм, именуемый Pf-CL145A, оказался многообещающим решением для контроля численности дрейссен. Этот бактериальный штамм, изолированный от внешней среды, может убить более 90 % дрейссен путём интоксикации (то есть, неинфекционно). Это происходит в результате действия натуральной субстанции(ий), входящей в состав их клеточных оболочек. С мертвыми клетками Pf-145A дрейссены погибают так же, как и с живыми. При очередном попадании в организм бактериальных клеток дрейссены гибнут вследствие последующего лизиса и некроза пищеварительной железы, а также отторжения некротических масс эпителия желудка. До настоящего момента исследования указывают на очень высокую специфичность в случае с дрейссенами, с низким риском нецелевого воздействия. Штамм Pf-CL145A в настоящий момент коммерциализирован под торговой маркой «Zequanox», который содержит его мёртвые бактериальные клетки в качестве активного ингредиента.
Этиология и распространение заболевания
В настоящее время возбудители этого заболевания уже хорошо изучены. Ими являются Pseudomonosis aeruginosa и Bacillus pyocyaneum. Эти разновидности синегнойной палочки отличаются высокой патогенностью. Во многом благодаря этому в природе они широко распространены. В серологическом плане они отличаются значительной вариабельностью. Эти микроорганизмы относятся к грамотрицательным. Возбудитель псевдомоноза представляет собой подвижную короткую палочку, которая может формировать цепочки. Длина этого микроорганизма составляет 0,8-1,4 ммк, а ширина — 0,4-0,6 ммк. Этот организм имеет всего 1 жгутик и до 10 ресничек. Оптимальной температурой для роста и увеличения численности синегнойной палочки считается +35°C…+37°C.
В действительности этот микроорганизм относится к условно-патогенным. Он нередко выявляется у абсолютно здоровых животных. Считается, что в большей степени к поражению синегнойной палочкой предрасположен молодняк, так как у него еще не до конца сформирован иммунитет. Помимо всего прочего, выделяется ряд внешних условий, которые способствуют поражению сельскохозяйственных животных. К таким факторам могут быть отнесены:
- нарушения санитарно-ветеринарных правил;
- повышенная влажность в помещении;
- несоблюдение профилактических перерывов эксплуатации инвентаря;
- нерациональное применение антибиотиков;
- использование низкокачественных кормов.
Все эти условия в значительной степени способствуют распространению инфекции. Обычно источником ее служат заболевшие животные, которые выделяют инфекцию во внешнюю среду вместе с калом, мочой, носовой слизью и даже молоком. Вполне возможно проникновение синегнойной палочки через плацентарный барьер. В этом случае молодняк может родиться с явными дефектами развития. Помимо всего прочего, резервуаром инфекции нередко выступают сухие и зеленые корма.
В настоящее время известно, что причиной стремительного распространения синегнойной палочки могут быть люди, которые нередко переносят этот патогенный микроорганизм на одежде, руках и предметах ухода за животными. На фермах, где разводится крупный рогатый скот, наиболее часто вспышки заболеваемости псевдомонозом диагностируются осенью. В хозяйствах, специализирующихся на выращивании домашней птицы и свиней, повышение заболеваемости наблюдается зимой. Некоторые исследователи связывают это со снижением иммунитета у животных.
Лечение
Лечение больных, находящихся в группе риска, проводят в стационарных условиях под постоянным контролем медицинского персонала. Все остальные больные в домашних условиях принимают лекарственные препараты по назначению лечащего врача. Самостоятельный выбор антибактериальных препаратов может привести к мутационной изменчивости возбудителя и появлению устойчивых штаммов. Специалисты назначают антибактериальные средства по данным антибиотикограммы – теста на чувствительность ко всем известным противомикробным препаратам. Их выбор обусловлен максимальной чувствительностью бактерий.
Антибактериальная терапия — цефалоспорины: «Цефтазидим», «Цефипим»; фторхинолоны: «Ципрофлоксацин», «Левофлоксацин»; монобактамы: «Азтреонам»; карбапенемы: «Имипенем», «Меропенем»; аминогликозиды: «Гентамицин», «Амикацин». Схему лечения с расчетом допустимой дозы, кратности приема лекарства и длительности определяет лечащий врач индивидуально каждому больному с учетом возраста, общего состояния и локализации патологического процесса.
Препараты бактериофагов вызывают гибель синегнойной палочки. Фаги лизируют бактерии и обладают гораздо меньшим количеством побочных эффектов, чем антибиотики. Этиотропная терапия — основа комплексного лечения инфекции.
Симптоматическая терапия направлена на устранения основных симптомов заболевания. Выбор препаратов определяется локализацией поражения.
- Жаропонижающие средства – «Нурофен», «Ибупрофен»;
- Обезболивающие препараты – «Кеторол», «Баралгин»;
- Антигистаминные средства – «Супрастин», «Цетрин»;
- Иммуномодуляторы – «Эсмиген», «Иммунал»;
- Про- и пребиотики – «Аципол», «Бифиформ»;
- Противодиарейных средств – «Имодиум», «Лоперамид»,
- Витаминно-минеральные комплексы.
Раны и инфицированные полости обрабатывают растворами антисептиков. При воспалении органов мочевыделения их промывают через вводимый катетер. Раны промываются по дренажу. Местное лечение также включает обработку гнойничков на коже противомикробными мазями, болтушками. После устранения острых явлений переходят к физиотерапии. При пневмонии, менингите и сепсисе показана дегидратационная и дезинтоксикационная терапия, заключающаяся во внутривенном введении коллоидных и кристаллоидных растворов. В тяжелых случаях может потребоваться хирургическое вмешательство для удаления сформировавшихся очагов, не поддающихся консервативному лечению.
Грамотное назначение лекарств обеспечивает быстрое восстановление пациентов без последствий и осложнений.
Metabolism
P. stutzeri is a facultative anaerobe that utilizes respiratory metabolism with terminal electron acceptors such as oxygen and nitrogen. When grown anaerobically, organisms within the genus Pseudomonas are considered to be model organisms for studying denitrification. Strains tested by Stainer and coworkers were able to grow and utilize the following substrates: gluconate, D-glucose, D-maltose, starch, glycerol, acetate, butyrate, isobutyrate, isovalerate, propionate, fumarate, glutarate, glycolate, glyoxylate, DL-3-hydroxybutyrate, itaconate, DL-lactate, DL-malate, malonate, oxaloacetate, 2-oxoglutarate, pyruvate, succinate, D-alanine, D-asparagine, L-glutamate, L-glutamine, L-isoleucine, and L-proline and hydrolysis of L-alanine-para-nitroanilide. D-maltose, starch, and ethylene glycol are carbon sources that are not commonly utilized by other pseudomonads as shown by Stainer et. al.
4 ответа
Не забывайте оценивать ответы врачей, помогите нам улучшить их, задавая дополнительные вопросы по теме этого вопроса.Также не забывайте благодарить врачей.
Агаджанова Ирина Юрьевналор 2016-12-01 17:45
Здравствуйте! Выделенная бактерия не опасна для вас и окружающих. Данный микроорганизм зачастую попадает в организм человека из кофемашин, через грязные руки. Хорошо размножается на фоне табакокурения. Сейчас достаточно орошения ротоглотки раствором Октенисепта, Мирамистина или Хлоргексидина 0,05% 3 раза в день в течение недели.
Ирина 2016-12-01 18:01
Спасибо огромное за быстрый ответ. Успокоили что не опасно для окружающих. Я переживала. Но все же не могу понять причины появления? Кофе пью только дома, заваренный в турке, из кофемашин не пила уже давно. Руки мою часто. Полоскала горло и мирамистином и хлоргексидином постоянно на протяжении вот этих двух месяце. Уже сил нет полоскать. Во рту очень сухо и губы постоянно трескаются, такого раньше не было. Может я уже наоборот всю нормальную флору пожгла и остались одни бактерии? Может надо как-то восстановить флору горла?
Агаджанова Ирина Юрьевналор 2016-12-03 15:33
Здравствуйте! Восстанавливать ничего не надо. Откуда появилась у вас это бактерия сказать сложно. Относительно сухих губ и сухости во рту следует проверить уровень глюкозы в крови и обследоваться у стоматолога и гастроэнтеролога.
Ирина 2016-12-04 19:08
Спасибо за ответ.
References
3. Montie, Thomas. Pseudomonas. New York: Plenum Press, 1998.
11. Hseuh, P., Teng, L., Pan, H., Chen, Y., Sun, C., Ho, S., and Luh, K. “Outbreak of Pseudomonas fluorescens Bacteremia among Oncology Patients” Journal of Clinical Microbiology, 1998. Volume 36, p. 2914-2917.
12. Rode, H., Hanslo, D., de Wet, P.M., Millar, A.J.W., and Cywes, S. “Efficacy of Mupirocin in Methicillin-Resistant Staphylococcus aureus Burn Wound Infection” Antimicrobial Agents and Chemotherapy, 1989. Volume 33, p. 1358-1361.
13. R. Srivastava, and S. “Antifungal Activity of Pseudomonas fluorescens Against Different Plant Pathogenic Fungi” The Internet Journal of Microbiology. 2009. Volume 7. Number 2.
Current Research
A copper-transporting P1-type ATPase (CueA) in the genome of Pseudomonas fluorescens SBW25 was investigated for its significance in copper homeostasis and plant colonization. The transcripton of cueA was induced by copper, silver , gold, and mercury ions by using a CueA-lacZ fusion. A nonpolar CueA deletion mutant that reduced its tolerance to copper by twofolds compared to the wild-type strain was also created for this experiment. This mutant did not show any change to its sensitivity to the gold, silver, and mercury ions. Its competitive ability was investigated by placing the mutant strain in three different environments which were a minimal M9 medium, the root of sugar beet (Beta vularis), and the root of pea (Pisum sativum). Change was not observed in the laboratory medium but were seen in the roots. This showed that CueA took part in copper homeostasis and contributed to bacterial fitness. (7)
1-aminocyclopropane-1-carboxylic acid (ACC) deaminase from Pseudomonas fluorescens was studied against saline stress in groundnut (Arachis hypogea) plants under in vitro and field conditions in which four plant growth-promoting rhizobacteria (PGPR) were used. The TDK1 strain was among the four and showed the most improvement in plant growth of the groundnut seedlings under in vitro conditions. Biochemical and molecular (PCR) analysis showed that strain TDK1 had the greatest ACC deaminase activity so it was isolated, cloned, sequenced, and tested under saline-affected soils in groundnut plants. Results showed improvement in yield even in the presence of saline. Therefore, Pseudomonas fluorescens strain TDK1 that contained ACC deaminase had increased yield by enhancing saline resistance. (8)
Using a universal Chrome Azurol S(CAS)-agar plate method, Pseudomonas florescens strain sp-f was isolated. Due to its nature of siderophore overproduction, experiments were performed to investigate the relationship between siderophores production and its growth. Siderophore production reached a peak during the prophase of logarithmic growth, then was stable during the stationary phase. From RP-HPLC analysis, three kinds of chatecholate siderophores were shown. While the excretion of non-fluorescent pyoverdin siderophores was induced by the 200 micromol/L Fe2+ in the medium, the excretion of fluorescent pyoverdin was completely repressed. (9)
Pseudomonas fluorescens produces an antibiotic called Mupirocin. A study was conducted with forty-five children who had MRSA infected burn wounds. MRSA was identified in the burn wounds of all forty-five children before the treatment began. A topical Mupirocin ointment was applied to the burn wounds twice a day and over a period of five day. The wounds were assessed daily. At the end of the clinical study, MRSA was eliminated in all 59 wounds. This study shows the great benefits of Mupirocin, especially against MRSA which is extremely resistant to a variety of antibiotics (12).