Грамотрицательные кокки семейства neisseria менингококки гонококки возбудители негонококковых
Содержание:
- Бактериальный менингит – симптомы, описание, особенности диагностики и лечения
- Менингит у детей
- Микробиологическая диагностика
- References
- Эпидемиология[ | код]
- Морфология[ | код]
- Лечение заболевания
- Клинические признаки гонококков у мужчин
- Neisseria meningitidis (менингококк)
- Факторы патогенности
- Pathogenesis
Бактериальный менингит – симптомы, описание, особенности диагностики и лечения
Бактериальный менингит – это острое воспаление мозговых оболочек, вызванное бактериями. Наиболее частым возбудителем менингита является бактерия neisseria Meningitidis или менингококк. Поэтому такой тип называют менингококковый менингит.
Самый распространенный возбудитель, вызывающий менингит – это менингококк. На его долю приходится до 80% всех случаев бактериального воспаления. И хотя существуют и другие возбудители, менингококк высеивается у человека практически всегда.
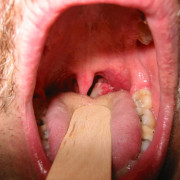
В норме он может жить в носоглотке человека. При этом человек может не иметь никаких клинических симптомов заражения. Если иммунитет ослабевает, возможно развитие менингококкового назофарингита. Он проявляется ринитом, заложенность в носу и болями в горле. Менингит при этом, как правило, не возникает.
Но если у человека снижен иммунитет, по каким-либо причинам, при заражении менингококком у него может развиться воспаление мозговых оболочек. Чаще всего этот вид менингита встречается у детей до 5 лет.
Передача возбудителя осуществляется при разговоре, кашле, чихании. А также, через зараженные возбудителем предметы.
Заболевание начинается остро, с внезапного развития симптоматики. Человек может с точностью назвать день и час, когда он заболел. Сопровождается бактериальное воспаление следующими симптомами:
- Повышение температуры тел до 38—39C.
- Ярко выраженная головная боль.
- Светобоязнь. Свет вызывает ухудшение самочувствия пациента. Больной старается спрятаться от источника света, натягивая одеяло себе на голову.
- Ригидность затылочных мышц. Для ее диагностики пациента просят дотянуться подбородком до груди. При наличии ригидности пациент сделать этого не сможет.
- Тошнота и рвота. Рвота не приносит облегчения.
- Оглушение. Пациент выглядит апатичным, плохо реагирует на звуки и обращение.
- Менингеальные синдромы.
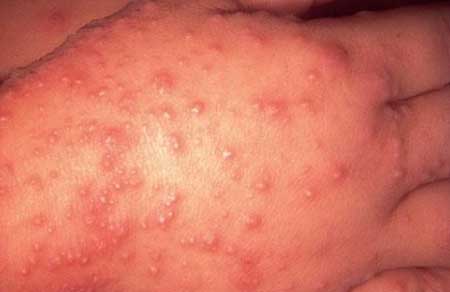
- «Звездчатая» сыпь на нижних конечностях. Этот симптом является признаком системного инфицирования (менингококцемия или менингококковый сепсис). Сыпь выглядит в виде синяков, по форме напоминающих звезды. Этот симптом является неблагоприятным прогностическим признаком.

У ослабленной группы больных и людей в пожилом возрасте симптомы протекают латентно.
При подозрении на бактериальный менингит пациента необходимо срочно госпитализировать. Если не предоставить пациенту необходимый объем медицинской помощи, то этот вид менингита смертелен.
Для диагностики используют:
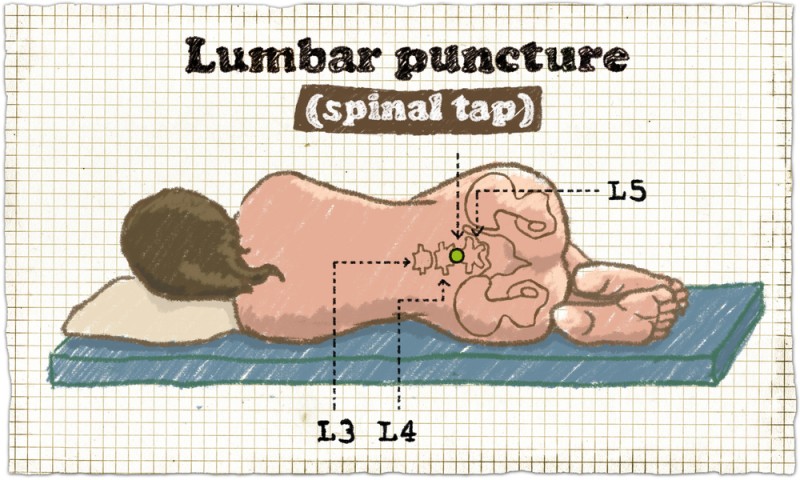
- Люмбальная пункция.
- ПЦР крови.
- Общеклинические исследования. Терапию начинают немедленно, не дожидаясь результата анализов.
Для лечения, до выявления возбудителя назначаются антибиотики (цефалоспорины, Ванкомицин).
Назначаются глюкокортикостероиды (гормональные препараты). Их прием необходим для уменьшения отека головного мозга.
Проводится массивная инфузионная терапия, поддержка кислородом. Как правило, пациенты поступают в отделение реанимации и интенсивной терапии.
Менингит у детей
Чаще всего менингитом болеют дети до 5 лет. Как правило, у них развивается бактериальный или вирусный менингит. Основную причину всех заболеваний занимает менингококк, а в случае с вирусным течением – энтеровирус, в том числе и вирус Коксаки.
Течение болезни в детском возрасте довольно тяжелое, встречается молниеносная форма инфекции. Для нее характерны симптомы ОРВИ (боль в горле, плохое самочувствие). Когда развиваются основные неврологические проявления, помочь пациенту уже нельзя.
Кроме этого, встречается и классическая менингеальная симптоматика. К ней относятся следующие клинические проявления и симптомы:
- головная боль;
- рвота фонтаном;
- ригидность затылочных мышц (в меньшей степени, чем у взрослых);
- выраженная лихорадка;
- синдром общей инфекционной интоксикации (слабость, утомляемость);
- светочувствительность и непереносимость звуков;
- «звездчатая» сыпь. Такая сыпь является одним из основных симптомов менингита у детей. Она появляется на нижних конечностях, а затем распространяется выше. Эта сыпь опасна тем, на месте высыпаний позже образуются участки некроза эпидермиса;
- положительные симптомы Кернига и Брудзинского;
- поза «легавой собаки», ребенок лежит на боку, ноги подведены к животу, а голова запрокинута назад;
- спутанность сознания. У маленьких детей пронзительный плач;
- отказ от груди или от пищи и жидкости.
Диагностика менингита у детей основывается на применении люмбальной пункции, взятии анализа крови для выявления возбудителя.
Дифференциальную диагностику проводят с вирусным менингитом воспалительными заболеваниями центральной нервной системы и другими инфекционными заболеваниями.
Для лечения менингита используются антибиотики широкого спектра действия до получения анализа на возбудителя. Кроме этого, проводится симптоматическая и поддерживающая терапия. Детям до 3-месячного возраста гормональные препараты не вводятся, но у детей более старшего возраста их назначение оправдано.
Особое внимание уделяется достаточному поступлению жидкости в организм ребенка. Для этого необходимо обеспечить обильное теплое питье, а при невозможности приема питья перорально, вводятся инфузионные растворы внутривенно-капельно
Иногда детей помещают в отделение реанимации для поддержания жизненно важных функций организма.
Прогноз при развитии менингита условно благоприятный. Летальность бактериального менингита составляет от 5 до 10%. У вирусного эти значения ниже.
Микробиологическая диагностика
Выбор материала для исследования обусловлен клинической формой болезни. Материалом для исследования служат носоглоточная слизь (от больных и носителей), ликвор, кровь, гной с мозговых оболочек, соскоб из элементов геморрагической сыпи на коже и др. При цереброспинальном менингите основным исследуемым материалом является ликвор, который берут в день госпитализации больного асептически люмбальной пункцией в количестве 2—5 мл. Ликвор собирают в стерильную пробирку и сразу же сеют на питательные среды или же немедленно, не допуская охлаждения, отправляют в лабораторию. Носоглоточную слизь берут специальным тампоном, изогнутым под углом, с задней стенки глотки при визуальном контроле, вводя тампон за мягкое нёбо. От трупа исследуемый материал (гной с оболочек мозга, из кожных поражений и т.п.) берут во время вскрытия. Поскольку менингококки очень неустойчивы вне организма человека, клинический материал транспортируют в утеплённых контейнерах при 30—35°С.
Для микробиологической диагностики применяют бактериоскопический, бактериологический и серологический методы.
Бактериоскопическое исследование ликвора и крови позволяет определить наличие возбудителя. При наличии гнойного ликвора готовят мазки без предварительной обработки; если ликвор прозрачный или мутный, его центрифугируют при 3500 об./мин. в течение 5 мин., а затем из осадка готовят мазки, которые окрашивают по Граму, метиленовым синим и другими методами для определения лейкоцитарной формулы, выявления менингококков и определения их количества. При микроскопии мазков ликвора в положительных случаях наблюдают полинуклеарные лейкоциты, эритроциты, нити фибрина и менингококки в виде типичных грамотрицательных диплококков бобовидной формы, окруженных капсулой в виде плохоокрашенного ореола. Результаты микроскопического исследования используются только в качестве предварительного, ориентировочного ответа, поскольку морфологически нельзя отдифференцировать менингококк от других грамотрицательных бактерий, способных вызывать менингит (гонококки, другие нейссерии, гемофилы, бранхамеллы). Для микроскопического исследования крови готовят препарат «толстой капли», который высушивают и окрашивают метиленовой синькой без фиксации. При микроскопии в положительных случаях обнаруживают на голубом фоне менингококки, имеющие типичную морфологию, окруженные капсулой в виде бесцветного ореола. Трупный материал исследуют только бактериоскопически из-за низкой жизнеспособности менингококка. Носоглоточная слизь не микроскопируется из-за наличия в ней условно-патогенных нейссерий, морфологически сходных с менингококком.
Бактериологическое исследование проводят с целью выделения и идентификации чистой культуры менингококка. Бактериологическому исследованию подвергают носоглоточную слизь, кровь и ликвор. Посев материала для получения чистой культуры производят на плотные или полужидкие питательные среды, содержащие сыворотку, кровь или асцитическую жидкость. Культуры инкубируют в течение 18—24 ч при 37°С в сосуде со свечой или в специальном термостате с повышенным содержанием (8—10%) CO2. Идентификацию выделенной культуры проводят на основании следующих свойств:
оксидазаположительные колонии рассматривают как возможно принадлежащие к видам Neisseria;
наличие в культуре Neisseria meningitidis подтверждают образованием уксусной кислоты при ферментации глюкозы и мальтозы (но не лактозы, сахарозы и фруктозы);
принадлежность к серогруппам определяют в реакции агглютинации (РА).
Проводят дифференциацию выделенной культуры с другими бактериями, вызывающими менингит. Серологический метод используют для обнаружения растворимых бактериальных АГ в ликворе и других видах исследуемого материала или AT в сыворотке крови. Для обнаружения АГ применяют ИФА, РИА, иммуноэлектрофорез, реакцию коагглютинации. У больных менингококковой инфекцией AT обнаруживаются с конца первой недели болезни, достигая максимума на 2—3-й неделе, а затем их титр снижается. У больных и лиц, перенесших ме-нингококковую инфекцию, в сыворотке обнаруживаются специфические AT: бактерицидные, агглютинины, гемагглютинины. В разгар менингококковой инфекции повышается уровень IgM, особенно при генерализованных формах; в период реконвалесценции, в основном, обнаруживаются IgG.
References
- Hitchcock P.J., Robinson E.N. (Jr.) and McGee Z.A., «Neisseriae: Gonococcus and Meningococcus», chap. 14 in Schaechter M., Medoff G. and Eisenstein B.I., Mechanisms of Microbial Disease, 2nd Ed., Baltimore, Williams & Wilkins, 1993., p.231.
- ^ Ryan, K.J.; Ray, C.G., eds. (2004). Sherris Medical Microbiology (4th ed.). McGraw Hill. pp. 329–333. ISBN 978-0-8385-8529-0.
- Critical Care Medicine. 27(10):2257-2261, OCTOBER 1999
- ^ , p. 1
- ^ (subscription required)
- Jarrell, K., ed. (2009). Pili and Flagella: Current Research and Future Trends. Caister Academic. ISBN 978-1-904455-48-6.
- Ullrich, M., ed. (2009). Bacterial Polysaccharides: Current Innovations and Future Trends. Caister Academic. ISBN 978-1-904455-45-5.
- ^
- Tunkel AR, Hartman BJ, Kaplan SL, Kaufman BA, Roos KL, Scheld WM, Whitley RJ (November 2004). «Practice guidelines for the management of bacterial meningitis». Clin Infect Dis. 39 (9): 1267–84. doi:. PMID .
- Genco, C.; Wetzler, L., eds. (2010). Neisseria: Molecular Mechanisms of Pathogenesis. Caister Academic. ISBN 978-1-904455-51-6.
- ^
Эпидемиология[ | код]
Экологической нишей для менингококка является слизистая оболочка носоглотки человека. Источник инфекции — больной человек или носитель. Различают три группы источников инфекции: больные генерализованными формами (около 1% от общего числа инфицированных лиц), больные назофарингитом (10—20% от общего числа инфицированных лиц) и здоровые носители. Основное значение имеют здоровые носители, которые составляют до 80—90%. Здоровое носительство у детей 1—2 лет встречается очень редко; с возрастом количество носителей нарастает, достигая максимума к 14—19 годам. Носительство продолжается в среднем 2—3 недели, при наличии хронических воспалительных процессов носоглотки может длиться 6 недель и более.
Механизм передачи — аэрогенный, путь — воздушно-капельный. В отличие от других респираторных инфекций заражение происходит при длительном и тесном контакте. Заболеваемость носит сезонный характер, увеличиваясь в осенне-зимний период.
Восприимчивость к менингококку невысокая. Болеют в основном дети до 15 лет (70—80%) и лица юношеского возраста (10—15%). Возникновению вспышек способствует скученность детей в детских организованных коллективах, учащихся школ и техникумов, студентов в общежитиях, новобранцев в казармах и т. п. Заболевания возникают при низком распространении носительства менингококка в коллективе (2% и ниже). В коллективах, где носительство составляет 20% и выше, заболевания не регистрируются, поскольку интенсивная циркуляция менингококка иммунологически перестраивает организм, обеспечивая «естественную иммунизацию» населения в эндемичных очагах заболевания.
В 2016 году учёные из Германии и Франции открыли новый штамм менингококка, инфицироваться которым возможно через мочеполовую систему. Эту разновидность микроорганизма также отличает от обычного штамма способность размножаться в условиях отсутствия кислорода.
«Менингитный пояс» | код
Распространение менингококкового менингита. Красным обозначен менингитный пояс Африки
Наибольшая распространенность этой болезни наблюдается в Африке в обширном менингитном поясе, расположенном к югу от Сахары, от Сенегала на западе до Эфиопии на востоке. В «менингитном поясе» расположены 26 стран, через которые проходит трансконтинентальная дорога, с которой связывают распространение менингококковой инфекции. Эпидемии отмечаются здесь через каждые 10—15 лет.
Этими 26 странами являются: Бенин, Буркина-Фасо, Бурунди, Демократическая Республика Конго, Гамбия, Гана, Гвинея, Гвинея-Бисау, Камерун, Кения, Кот-д’Ивуар, Мали, Мавритания, Нигер, Нигерия, Руанда, Сенегал, Судан, Танзания, Того, Уганда, Центральноафриканская Республика, Чад, Эритрея, Эфиопия, Южный Судан. Уровень риска эпидемии менингококкового менингита в этих 26 странах и между разными странами колеблется в широких пределах.
Морфология[ | код]
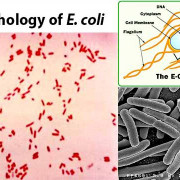
Клетки округлые диаметром 0,6—1,0 мкм, располагаются попарно. Поверхности, обращённые друг к другу, вогнутые или ровные. Клетки полиморфны. Грамотрицательны, но отношение к окраске по Граму выражено недостаточно чётко, поэтому в мазках наблюдается неравномерное окрашивание — молодые клетки окрашиваются интенсивно, а отмирающие и мёртвые клетки — очень слабо. Жгутиков не имеют, спор не образуют. Клинические изоляты образуют макрокапсулу, которая утрачивается при росте на питательных средах.
Культуральные свойства | код
Строгий аэроб, капнофил. Очень требователен к питательным средам и условиям культивирования. На простых питательных средах не растёт, поэтому для его культивирования к основным средам добавляют нативные белки (сыворотка, кровь, яичный желток и др.). В качестве источников углерода и азота используют аминокислоты (глутамин, таурин, аспарагин, L-аргинин, глицин, тирозин), поэтому их необходимо включать в среду культивирования. Наиболее подходящей бессывороточной средой следует считать среду Мюллера-Хинтона, включающую полный набор аминокислот и мясной экстракт как источник факторов роста. Оптимум рН среды 7,2—7,4. Температурный оптимум роста 37°С, рост наблюдается в пределах 30-38°С. Повышенная концентрация СO2 и влажность стимулируют рост менингококков. На сывороточном агаре образует круглые бесцветные нежные колонии маслянистой консистенции диаметром от 0,5 до 1,5 мм. В отличие от условно-патогенных нейссерий не образует пигмента. На кровяном агаре образует нежные округлые колонии слегка сероватого цвета с блестящей поверхностью. Не даёт гемолиза, что отличает его колонии от колоний стафилококков, стрептококков и гемофилов. При первичном посеве очень требователен к условиям культивирования, поэтому отсутствие роста на бессывороточном агаре при 37°С, на сывороточном агаре при 20°С и среде с 5% жёлчи дифференцируют менингококки от условно-патогенных нейссерий.
Лечение заболевания
Благодаря современной медикаментозной терапии гонорея полностью излечима. Бактерий уничтожают с помощью антибиотиков, при этом лечение продолжается всего несколько дней.
При неосложненных формах врач-венеролог назначает следующие препараты:
- Цефтриаксон – 250 мг внутримышечная инъекция 1 раз в сутки;
- Офлоксацин – 400 мг 1 раз в сутки;
- Норфлоксацин – 800 мг 1 раз в сутки;
- Ципрофлоксацин – 500 мг 1 раз в сутки.
Поскольку гонококковая инфекция в 30% случаев протекает параллельно с заражением хламидиями, то при их выявлении дополнительно назначают препараты:
- Азитромицин 1 г внутрь разово;
- Доксициклин – 100 мг 2 раза в сутки.
При осложненном протекании заболевания больной проходит лечение в стационаре. Такая терапия бывает более продолжительной.
Больному назначают постельный режим. Кроме того, во время лечения он должен избегать вредных привычек, иначе терапия будет неэффективной.
Антибиотики, которые назначают при продолжительном курсе лечения, относятся к ряду фторхинолонов:
- Ципрофлоксацин – 500 мг 2 раза в сутки;
- Цефтриаксон – 1 г внутримышечно или внутривенно 1 раз в сутки;
- Цефотаксим – по 1 гр. внутривенно 3 раза в сутки.
Продолжительность курса зависит от протекания болезни, состояния организма пациента и назначается врачом.
В среднем лечение занимает от 2 до 7 дней. Дополнительно в терапевтический курс вводят физиопроцедуры: лечение лазером, грязелечение, электрофорез с противовоспалительными средствами и ряд других, что помогает быстрее преодолеть болезнь.
Лечиться от венерического заболевания должны оба партнера. Это позволит избежать вторичного заражения и сократить риск осложнений. Следует сообщить своему партнеру о болезни и совместно пройти диагностику, даже если никаких подозрительных симптомов напарник не ощущает.
После лечения в половую связь можно вступать спустя 5 суток, но использование презерватива обязательно. Некоторые полагаются на медикаментозное лечение.
Оно эффективно, но часто к нему прибегать вредно. Не следует заменять презерватив на медикаменты: это не одно и то же.
Лечение антибиотиками (без осложнений) непродолжительно, поэтому отрицательные последствия в виде дисбактериаоза, кандидоза не проявляются.
Более длительный курс предполагает побочные эффекты, которые есть у этой группы препаратов. Но надежность такого лечения равна 100%.
Клинические признаки гонококков у мужчин
Инкубационный период у представителей мужского пола короче, чем у женщин, и длится в пределах 2-3 дней.
Признаки триппера развиваются в зависимости от пораженного участка и локализации воспалительных процессов.
Как правило, у мужчин в первую очередь гонококки поражают мочеиспускательный канал.
В результате чего развиваются симптомы:
- из уретры выделяются гнойное содержимое;
- при мочеиспускании больной испытывает сильные боли;
- половой акт сопровождается болезненными и дискомфортными ощущениями;
- одним из симптомов поражения гонококками является формирование язв на члене.
В большинстве случаев при дальнейшем распространении инфекционных процессов страдает предстательная железа.
Воспалительные явления в ней имеют острое и хроническое течение.
Симптомы гонококков в простате зависят от формы простатита:
- Катаральный (поражаются дольки предстательной железы) – учащаются походы в туалет, в процессе опорожнения мочевого пузыря возникает жжение, в промежности появляется незначительный зуд, в анальном отверстии ощущается давление. При мочеиспускании моча имеет нитевидные примеси гноя. В анализе секрета простаты обнаруживается большая концентрация гонококков.
- Фолликулярный (образовываются гнойные уплотнения) – в паху и промежности беспокоит постоянное ощущение жара, при опорожнении мочевого пузыря выраженные боли возникают лишь в конце процесса. При ректальном пальцевом исследовании отмечается увеличение воспаленного органа в размерах, прощупываются шарообразные уплотнения, внутри которых присутствует гной.
- Паренхиматозный (формируется абсцесс внутри органа) – мочеиспускание затруднено, может развиваться острая задержка мочи, в области ануса постоянно ощущается сильное давление, процесс дефекации сопровождается выраженными болями, которые отдают в половой член, тазовую область и нижнюю часть позвоночного столба.
Хронические процессы сопровождаются такими признаками, как:
- эректильные дисфункции;
- преждевременное семяизвержение;
- снижение ощущений при половом контакте.
Neisseria meningitidis (менингококк)
Менингококк (Neisseria meningitidis) — вид грамотрицательных споронеобразующих бактерий из рода нейссерий, возбудителей менингита и других менингококковых инфекций человека. Имеют форму шаров (кокков) диаметром от 0,6 до 1 мкм. Часто располагаются попарно, из-за чего называются диплококками.
Менингококковый менингит
Наиболее часто Neisseria meningitidis ассоциируют с вызываемым ими опасным заболеванием человека, инфекцией тонкой оболочки мозга, окружающей головной и спинной мозг — менингококковым менингитом, тяжелому поражению мозга, которое при отсутствии лечения в половине случаев заканчивается летальным исходом. Кроме Neisseria meningitidis бактериальный менингит могут вызывать Haemophilus influenzae, Streptococcus pneumoniae и другие бактерии.
Существует целый ряд (более 10) серогрупп менингококков. Возбудителями менингококковой инфекции являются серогруппы А, В, С, X, Y и W135.
Менингококк передается от человека человеку через капельные выделений из дыхательных путей или горла носителя. Распространению инфекции способствуют поцелуи, чихание или кашель, пользование общей посудой, проживание в общей спальне. Инкубационный период продолжается обычно от двух до десяти дней, но чаще всего около четырех дней.
Резервуаром менингококков являются только люди. Neisseria meningitidis могут переноситься в горле, и по не выясненным причинам, распространяется через кровоток в мозг.
Наибольшее количество случаев заболевания менингококкового менингита отмечается в так называемом менингитном поясе в Африке к югу от Сахары, идущем от Сенегала на западе до Эфиопии на востоке.
Эффективным способом профилактики менингококкового менингита является вакцинирование. В 2005 году в США, а затем и в других странах (в России — в 2014 году), получила разрешение на применение четырехвалентная менингококковая конъюгированная вакцина MenA для лиц от 2-х до 55 лет против серогрупп А, C, Y и W. В конце октября 2014 г. FDA одобрило для медицинского применения в США первую вакцину, предназначенную для предотвращения распространения менингококковой инфекции у лиц с 10 по 25 лет, вызванную Neisseria meningitidis серогруппы B.
Лечение менингита производят в стационаре, антибиотиками, которые должны вводиться больному как можно скорее. Могут применяться: пенициллин, ампициллин, хлорамфеникол и цефтриаксон и другие. Из представленных в настоящем справочнике в отношении Neisseria meningitidis активны: ципрофлоксацин, норфлоксацин, офлаксацин, кларитромицин, джозамицин (в высоких концентрациях), амоксициллин, рифабутин, рокситромицин.
Менингококковые инфекции в МКБ-10
Международная классификация болезней МКБ-10 содержит в «Классе I Некоторые инфекционные и паразитарные болезни (A00-B99)», блоке «A30-A49 Другие бактериальные болезни» трёхсимвольную рубрику «A39 Менингококковая инфекция», в которую входят следующие коды:
A39.0 Менингококковый менингит. A39.1 Синдром Уотерхауса-Фридериксена (менингококковый геморрагический адреналит, менингококковый адреналовый синдром). A39.2 Острая менингококкемия. A39.3 Хроническая менингококкемия. A39.4 Менингококкемия неуточненная (менингококковая бактериемия БДУ). A39.5 Менингококковая болезнь сердца (менингококковый: кардит БДУ, эндокардит, миокардит, перикардит). A39.8 Другие менингококковые инфекции (менингококковый: артрит, конъюнктивит, энцефалит, неврит зрительного нерва; постменингококковый артрит). A39.9 Менингококковая инфекция неуточненная.
Факторы патогенности
Основной фактор патогенности — капсула, защищающая менингококки от различных воздействий, в первую очередь от фагоцитоза. AT, образующиеся к полисахаридам капсулы, проявляют бактерицидные свойства. Токсические проявления менингококковой инфекции обусловлены высокотоксичным эндотоксином, который по летальности для лабораторных животных сравним с эндотоксинами энтеробактерий. Оба они оказывают сенсибилизирующее действие и индуцируют феномен Шварцмана в концентрациях, в 5—10 раз меньших, чем ЛПС грамотрицательной кишечной микрофлоры. Для генерализованных форм менингококковой инфекции характерны кожные высыпания, неотличимые от таковых при феномене Шварцмана. ЛПС менингококков проявляют выраженное пирогенное действие, а также вызывают образование AT. Тяжесть болезни определяется количеством эндотоксина в крови больного. Эндотоксину принадлежит ведущая роль в патогенезе поражений сосудов и кровоизлияний во внутренние органы. Наиболее постоянный и диагностически значимый признак менингококцемии — экзантема в виде характерной геморрагической сыпи (петехии, пурпура, экхимозы).
К другим факторам патогенности относятся пили, белки наружной мембраны, наличие гиалуронидазы и нейроминидазы. Пили являются фактором адгезии к слизистой оболочке носоглотки и, предположительно, тканям мозговой оболочки. Менингококки выделяют IgA-протеазы, расщепляющие молекулы IgA в шарнирной области, что защищает бактерии от действия Ig.
Лабораторные животные мало восприимчивы к менингококку. Субдуральное введение живой культуры может вызвать заболевание у кроликов, обезьян и коз. Внутрибрюшинное заражение белых мышей и морских свинок вызывает их гибель с явлениями интоксикации. Заражение в аллантоисную полость 11—18-дневных куриных эмбрионов вызывает гибель эмбриона через 48 ч.
Pathogenesis
Virulence
Lipooligosaccharide (LOS) is a component of the outer membrane of N. meningitidis. This acts as an endotoxin and is responsible for septic shock and hemorrhage due to the destruction of red blood cells. Other virulence factors include a polysaccharide capsule which prevents host phagocytosis and aids in evasion of the host immune response; fimbriae mediate attachment of the bacterium to the epithelial cells of the nasopharynx. It infects the cell by sticking to it mainly with long thin extensions called pili and the surface-exposed proteins Opa and Opc. Meningococci produce an IgA protease, an enzyme that cleaves IgA class antibodies and thus allows the bacteria to evade a subclass of the humoral immune system.
A hypervirulent strain was discovered in China. Its impact is yet to be determined.
Complement inhibition
Factor H binding protein (fHbp) that is exhibited in N. meningitidis and some commensal species is the main inhibitor of the alternative complement pathway. fHbp protects meningococci from complement-mediated death in human serum experiments, but has also been shown to protect meningococci from antimicrobial peptides in vitro. Factor H binding protein is key to the pathogenesis of N. meningitidis, and is, therefore, important as a potential vaccine candidate. Porins are also an important factor for complement inhibition for both pathogenic and commensal species. Porins are important for nutrient acquisition. Porins are also recognized by TLR2, they bind complement factors (C3b, C4b, factor H, and C4bp (complement factor 4b-binding protein)). Cooperation with pili for CR3-mediated internalization is another function of porins. Ability to translocate into host cells and modulate reactive oxygen species production and apoptosis is made possible by porins, as well. Strains of the same species can express different porins.