Ветврачи подмосковья начали отрабатывать процедуры диагностики паратуберкулеза у скота
Содержание:
- Общие характеристики
- Pathology
- симптомы
- Cell structure and metabolism
- Classification
- Профилактика
- ссылки
- Ecology
- Симптомы заболевания
- Источники и пути инфицирования
- Симптоматика паратуберкулезного энтерита
- Микобактериоз легких: основные сведения, причины, симптомы, методы лечения
- Симптомы течения паратуберкулеза
- Представители рода микобактерий
- морфология
- Genome structure
- Pathophysiology
- Как лечить животных, инфицированных паратуберкулезом
- Диагностика болезни
Общие характеристики
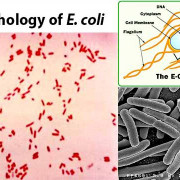
Как уже упоминалось, Mycobacterium avium комплекс это группа бактерий, которые имеют много общих характеристик.
Это аэробные организмы
Эти бактерии обязательно должны находиться в среде с широкой доступностью кислорода. Они требуют, чтобы этот химический элемент мог выполнять свои метаболические процессы.
Они медленно растут
Бактерии Mycobacterium avium комплекс Они очень медленно растут. В культурах в твердых средах прохождение колоний занимает 10-21 день. Это потому, что они синтезируют длинноцепочечные жирные кислоты (60-80 атомов углерода), которые интегрируют их внешнюю мембрану.
среда обитания
Эти бактерии характеризуются их повсеместным распространением. Это подразумевает, что их можно найти в любой точке мира. Эти бактерии были изолированы во многих средах, таких как пыль, вода и различные животные.
Они патогенные
Этот тип бактерий способен вызывать патологии как у животных, так и у людей. В случае человека, он нападает как на иммунокомпетентных, так и на людей с подавленным иммунитетом.
Это особенно оппортунистический организм у людей, инфицированных вирусом приобретенного иммунодефицита (СПИД).
Они каталазы положительные
Бактерии Mycobacterium avium комплекс Они синтезируют фермент каталазы, который позволяет им разрушать молекулу перекиси водорода (H2О2в воде и кислороде. Это важная характеристика, которая позволяет идентифицировать и дифференцировать бактерии на экспериментальном уровне.
Они негативные уреазы
Эти бактерии не синтезируют фермент уреазы, поэтому они не способны гидролизовать мочевину с получением аммиака и углекислого газа..
Они не фотохромные
Фотохромогенные бактерии — это те, чьи культуры при воздействии света вырабатывают каротиноидные пигменты интенсивного желтого цвета..
Они Ziehl — Nielsen положительный
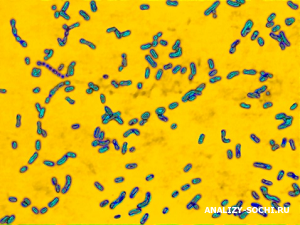
Из-за своего кислотоустойчивого статуса бактерий наиболее часто используемым пятном для их наблюдения является окраска Циля-Нильсена. При этом бактериальный образец подвергается красному красителю, а затем добавляется метиленовый синий, чтобы сделать контраст.
Наблюдая за ними под микроскопом, можно увидеть синий фон и на этом красные палочки, соответствующие Mycobacterium avium комплекс.
Устойчивость к антибиотикам
Бактерии Mycobacterium avium комплекс обладают устойчивостью к следующим антибиотикам: изониазид, этамбутол, рифампицин и стрептомицин.
Pathology
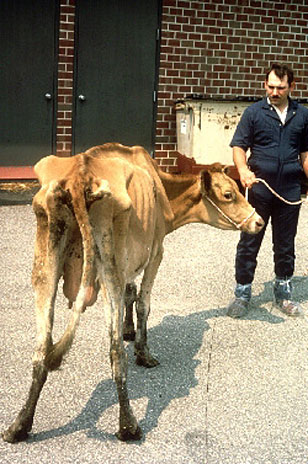
Mycobacterium avium subspecies paratuberculosis is pathogenic in mammals; it is the causative agent of Johne’s disease or paratuberculosis. Map primarily infects ruminants and pseduoruminants including but not limited to cattle, sheep, goats, dear, antelope, bison and llama . Though it is most common found in these animals, it is definitely not restricted to these species, seeing that is has been found in many wild badger, fox, primates, rabbits, swine, and weasels . Infection has been found to readily spread between and across species with no restrictions, making the disease hard to control. Wild animals are proposed to be one method by which transfer of the Map bacterium occurs between farms or herds. Young animals are most susceptible to infection by Map because adults require a higher level of exposure to the bacteria in order to progress toward the disease . Neonates are also at high risk of infection by their mother’s milk or contact with the bacteria during birth. Animals are most likely to be infected through the fecal-oral route due to contamination of water and food supplies by infected feces.
Johne’s disease progression has four stages: silent infection, subclinical, clinical, and advanced clinical disease. Once ingested, Map established itself in the lymphoid tissue of the upper gastrointestinal tract . Clinical and visible manifestations of the disease will not be apparent for 1 to 10 years following infection, again making the disease hard to detect . During that time, some of the Map is engulfed by epithelioid macrophages which elicit lymphocyte activation and clonal expansion. The immune system first responds with a Th1 response; a production of gamma interferon, interleukin 2, and tumor necrosis factor-alpha cytokines. This is followed by the Th2 response, wherein the animal begins to show nonspecific signs of disease, including weight loss and diarrhea despite a normal diet. These symptoms are due to pathogenic changes which occur throughout the disease progression. Proteins released from Map into the ileum lead to thickened and corrugated tissue as well as edematous lymph nodes. The inflammatory cells which respond to such an infection cause the intestinal wall to thicken until it can no longer function, thus leading to malabsorption and protein-losing enteropathy. Once animals have reached the advanced clinical phase, they usually die within weeks .
Because of non-specific clinical signs and long periods disease incubation withing the host animal, testing and management for control pose the greatest problem of this rapidly spreading disease. Diagnosis has been determined most effective when reviewing an entire herd rather than an individual by the pooling of clinical samples. All forms of testing unfortunately require a great amount of time and expense . Vaccination has been deemed ineffective and economically impracticable ; though it can decrease the rate of disease, it cannot prevent infection and it has also been found to alter the results of tuberculosis testing, another major problem for cattle herds . Though there is currently no cure for Johne’s disease, surveillance and control programs are being established throughout the globe that are committed to determining the location, species, familial links, and exposure history of any animals with confirmed disease in hopes to one day take control of this devastating disease and its etiologic agent Map .
симптомы
лимфаденит
Характеризуется безболезненным увеличением размеров лимфатических узлов, в частности шейных и подчелюстных лимфатических узлов. Там нет никаких других симптомов или признаков, в том числе лихорадка.
Болезнь легких
Это патология, сходная с туберкулезом, но в отличие от нее она не заразна от человека к человеку. Среди его симптомов:
- Постоянный продуктивный кашель
- Общее недомогание
- усталость
- лихорадка
Распространенная болезнь
Эта патология является следствием распространения бактерий по всему организму, через кровоток. У людей со здоровой иммунной системой обычно нет.
Это очень часто встречается у людей с подавленной иммунной системой, особенно у ВИЧ-инфицированных. Среди его наиболее характерных симптомов упоминаются:
- Высокая температура
- исхудание
- Ночные поты
- усталость
- понос
- Боль в животе
Cell structure and metabolism
Map is a small, slow-growing, gram-positive, acid-fast positive, rod-shaped, multispecies pathogenic bacteria. It is aerobic, has no mechanisms of motility and has a cell wall made up of a waxy mixture of lipids and polysaccharides . The cell wall of a pathogen must act as an interface between the cell and its host, and thus will structurally display that parasite’s virulence. In the case of Map, a thick waxy cell wall made up of 60% complex lipids not only gives it the properties of an acid fast bacteria (the ability to resist decolorization by acidified alcohol), but it also creates hydrophobicity and an increased resistance to low pH, high temperature, and a variety of chemicals, increasing its longevity and pathogenic potential in harsh and varied environments . Studies have shown that virulence may be increased in Map by the presence of two copies of the five genes (fabG2, accD4, kasB, fabG3 and fabG5) involved in the fatty acid biosynthetic pathway through the combined action of these fatty acid synthases and polyketide synthases to create the complex lipid components of the membrane .
A thick cell wall also contributes to the slow growth rate of Map by decreasing the flow of nutrients into and out of the cell. Map is actually the slowest growing of all cultivated mycobacteria; under optimal conditions, it takes over 20 hours to generate. A Map isolate can produce small colonies within 3-6 weeks when grown in the optimal temperature of 37 degrees C under aerobic conditions . As an aerobic organism, Map requires oxygen in its environment for metabolism; in order to survive in low-oxygen environments, it produces isocitrate lyase, an essential anapleurotic enzyme which assists in survival within microaerophilic conditions inside the host. In terms of metabolism, Map has a functional glycolytic pathway and tricarboxylic acid (TCA) cycle. The presence of an additional FAD binding domain in the fdhF gene, and the intact iron-sulfur domain within the fdxB gene possibly indicate an alternate survival strategy for Map which would be similar to that of the anaerobic survival of M. Tuberculosis under starvation .
Mycobactin is a siderophore unique to the mycobacterial family. This chemical is secreted from the membrane in order to break down and transport iron (an essential nutrient for growth) into the cell. Map is unique in that it does not produce mycobactin on its own like the rest of its genus, and thus requires a host cell to provide iron, which normally comes from cell macrophages. Because of this, in order to grow Map cells in in vitro culture, they must be provided with mycobactin in the medium or they will not grow or reproduce . This mycobactin deficiency can also be seen as a contributor to the bacteria’s slow growth rate .
Classification
Higher order taxa
Bacteria (Domain); Actinobacteria (Phylum); Actinobacteria (Class); Actinobacteridae (Subclass); Actinomycetales (Order); Corynebacterineae (Suborder); Mycobacteriaceae (Family); Mycobacterium (Genus); Mycobacterium avium complex (MAC) (Species group)
Mycobacterium avium subspecies paratuberculosis
Commonly referred to as MAP or Map
Also known as: Mycobacterium paratuberculosis, Mycobacterium johnei, Bacillus paratuberculosis, Bacterium paratuberculosis, Mycobacterium enteritidis, Darmtuberculose, and Mycobacterium avium paratuberculosis
The classification of this organism has been subject to debate. Isolated over 100 years ago, it was originally termed Mycobacterium enteritidis chronicae pseudotuberculosae bovis johne . Current classifications depend on genetic composition and phenotypic characteristics. With a genome almost identical to that of Mycobacterium avium (M. avium) and its subspecies, the International Association for Paratuberculosis has recognized the subspecies term (Map) as fitting. On the other hand, some researchers and organizations still use the name M. paratuberculosis, not only for simplicity, but as a result of its significant phenotypic variances from M. avium .
Профилактика
В неблагополучных по паратуберкулезу районах коров периодически осматривают. Животных с видимыми симптомами сдают на убой. Всех остальных, которым уже исполнилось 1,5 года, подвергают диагностике с помощью РСК. Тех, у кого выявлены положительные пробы, также сдают на убой, с отрицательными результатами оставляют в стаде. Затем этих коров обследуют тем же методом дважды в год.
Телят до 1,5 года выращивают отдельно от остального стада. Кормят молоком здоровых животных или молоком от тех, которые имеют положительные пробы, но нет клинических признаков паратуберкулеза. Такое молоко предварительно пастеризуют.
Приобретать новых животных для комплектования стада нужно только из благополучных по этому заболеванию хозяйств, ведь не всегда видно, что корова или теленок больны. Кормить животных и обеспечить им уход нужно в соответствии с зоогигиеническими требованиями. После уборки навоза его нужно высушивать и сжигать или биотермически обеззараживать в компостных кучах.
Проводить дезинфекцию помещений, где содержатся коровы, инвентаря и доильного оборудования. В качестве дезинфекторов можно использовать гашеную известь, гидроксид натрия, раствор формальдегида, креолина, фенола. Дезинфицируют коровники после обследования поголовья и после отелов. Хозяйство считается благополучным по паратуберкулезу, если в нем проводились санитарные обработки, и в течение 3 лет после последнего случая заболевания не было выявлено больных животных.
Паратуберкулез КРС не лечится, больные животные либо умирают, либо их сдают на убой. Чтобы не допустить распространения болезни внутри хозяйства, нужно проводить осмотры поголовья, делать анализы, позаботиться о том, чтобы можно было выращивать коров отдельно от общего стада, если понадобится.
ссылки
- Сеспедес, М. и Аберг, J. Mycobacterum avium комплекс. Получено с: antimicrobe.org.
- Horsburgh, C. (1991). Mycobacterium avium комплекс инфекция в синдроме приобретенного иммунодефицита. Медицинский журнал Новой Англии. 324. 1332-1338.
- Mycobacterium avium комплекс. Получено от: Microbewiki.kenyon.edu
- Салдиас Ф., Тирапеги Ф. и Диас О. (2013). Легочная инфекция Mycobacterium avium комплекс в иммунокомпетентном хозяине. Чилийский журнал респираторных заболеваний. 162-167
- Сантос, М. и Гобернадо, М. Микобактериальный комплекс: микробиологические аспекты. Получено с: seimc.org
- Севилья, I. (2007). Молекулярная характеристика, обнаружение и устойчивость Mycobacterium avium подвид паратуберкулеза. Получено от: Euskadi.es
- Сурко В. и Гавинча С. (2014). Микобактерии. Журнал клинических обновлений и исследований. 49.
Ecology
Map and protozoa. Many studies have been done to test the intracellular growth patterns of M. avium within environmental protozoan hosts. By interfering with the fusion of lysosomal and parasitophoric vacuoles within the protozoa, many bacteria are able to survive, if not thrive, within these organisms. It has been found that the uptake of M. avium by certain amoeba (for example Acanthamoeba castellanii) creates a protective barrier for the bacteria, keeping it safe from antibiotics and harsh environmental factors. Some pathogenic amoebae have the ability to traverse the intestinal epithelium; and thus can carry encapsulated mycobacteria along for the ride (for this reason, some have called this a Trojan horse relationship). The bacteria can be released and transported by the amoeba through cysts which are created on the outside of the protozoa and are carried by the wind. Further studies have found M. avium replication and virulence to be enhanced after growth inside amoebae. Though limited research has been done to test these relationships in Map, its similarities to M. avium create a good starting point. Studies have shown similar results for Map in lab cultures (protozoan engulfment leading to protection and enhanced survival), but have yet to test the interactions between protozoa and Map in the natural environment, where temperatures are lower and there may be other outside factors to take into account . If, in further studies, this turns out to be a significant relationship, it will open the door for a new niche outside of the infected animal wherein Map can successfully replicate and be distributed .
Map, nematodes and insects. Studies have been done to test the interactions between Map and nematodes, earthworms, cockroaches, as well as Diptera (flies). All of these organisms live near and within possibly contaminated soil and faeces. Earthworms were found to have the smallest contribution to Map transfer because the bacteria could only survive within their systems for about two days. Map was found to be closely associated with nematode larval bodies, which are able to penetrate the gastrointestinal mucosa, creating a good means of transfer of environmental Map into host animals that eat the third stage larvae from the grass. Because of the hardy structure of the mycobacterial cell walls, Map is resistant to the digestive enzymes of insects which consume them, thus creating an additional pathway of infection. Diptera, which injest fluids from cut intestines in slaughterhouses which may be contaminated with Map, similarly were found important in the spread of Johne’s disease within infected herds .
Map and the environment. Though Map is an intracellular parasite which requires a host for replication and growth, it does not require a host for survival, and thus has been found in many areas of the environment and is highly resistant to many environmental conditions. It has been found to be prevalent in soil, pond water and pastures to which infected cattle may have access (for contamination by feces). A study in 1944 showed Map survival in outdoor manure to last 246 days. In water of pH 7.0 it lasted up to 17 months. Map is tolerant to high temperatures, which decreases the effectiveness of pasteurization to kill the organism in infected milk. Studies concerning Map resistance to ultraviolet (UV) light have resulted in uncertain and inconclusive results . So far, Map has not been isolated from any biofilm formations, but other mycobacteria have. Biofilms create a resistance to environmental stresses for all those organisms within the watery congregation, thus it is a good area for future research of Map ecology .
Симптомы заболевания
Инкубационный период паратуберкулеза может длиться от нескольких месяцев до 1 года. Болеющие латентно коровы отстают в росте, худеют, причем упитанность не восстанавливается. Те животные, которые отличаются неплохой сопротивляемостью организма и которые нормально питаются и получают хорошее содержание, могут выздоравливать самостоятельно. Латентно протекающая болезнь переходит в клиническую форму по различным причинам, которые уменьшают резистентность организма коров.
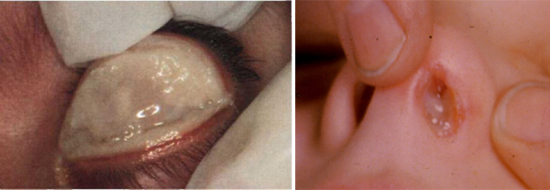
Определить паратуберкулез можно по таким первым его признакам, как снижение удоев, появление отеков под челюстью и в зоне подгрудка, прогрессирующее истощение. Периодически у животных случается диарея, с течением времени она приобретает стойкий характер. Фекалии жидкой консистенции, имеют неприятный запах, в них можно заметить комочки слизи, редко – кровь и пузырьки газа. Животные нормально едят, не теряют аппетит, но из-за обезвоживания организма начинают пить больше воды. Повышения температуры и болей не наблюдается.
Корова худеет, уменьшается мышечная масса, особенно на крупе и задних ногах. Это снижает экономическую ценность животного.
Источники и пути инфицирования
Бактерии попадают в организм коров с пищей, которая заражается фекальными массами и выделениями больных животных, так как у коров при паратуберкулезе пораженным оказывается кишечник. Микобактерии могут оказаться на инвентаре по уходу за животными, ими могут быть заражены пастбища, источники воды, фураж и помещения. Телята заражаются через молоко от больных матерей, а также могут рождаться уже инфицированными.
Выделение паразитов из организма больных животных начинается спустя 3-5 месяцев после заражения. Опасен паратуберкулез тем, что многие животные болеют бессимптомно, из-за чего по внешнему виду не отличаются от здоровых, но являются носителями бактерий.
Вспышки паратуберкулеза могут приходиться на любой период года. Большое количество заболеваний регистрируется в регионах, где кислые, влажные или солончаковые почвы, что объясняется тем, что выросшие на таких почвах растения бедны солями кальция и фосфора.
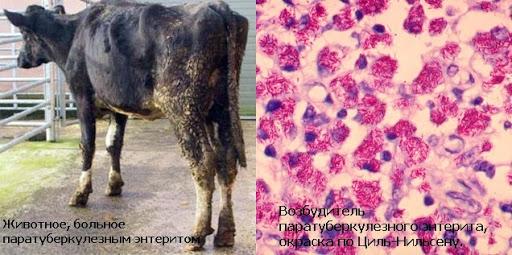
Вероятность развития паратуберкулеза увеличивается при кормлении коров кислыми кормами, например, силосом, при глистных инвазиях, после переохлаждения или перегревания животных. Коровы могут заболевать в период акклиматизации или при содержании в непривычных условиях.
Симптоматика паратуберкулезного энтерита
Основными признаками инфицирования паратуберкулёзом крупного рогатого скота являются понос и истощение. Стоит заметить, что зачастую симптоматика проявляется примерно в 2-6-летнем возрасте, несмотря на то что заражение происходит ещё в течение первого года жизни, а иногда в период внутриутробного развития.
На раннем этапе развития паратуберкулёзного энтерита симптоматика слабовыраженная. Чаще всего клиническая картина заболевания проявляется снижением массы тела, понижением производительности и незначительной взъерошенностью шерстяного покрова. Выделение каловых масс наблюдается немного чаще чем обычно, но фекалии достаточно густые, эпителиальные остатки, кровь и слизь отсутствуют. Систематически пищеварительные функции стабилизируются.
Спустя некоторое время после возникновения поноса у коров отмечается отёчность мягких тканей в области нижней челюсти. Такой признак называют «бутылочной челюстью» либо «межчелюстным отёком». Объясняется это выведением белков из кровотока на фоне расстройства пищеварительных функций.
Дальнейшее прогрессирование болезни приводит к ещё большему снижению веса у животного. Также наблюдается обезвоживание в сочетании с тяжёлой кахексией, из-за чего корова гибнет.

Признаки обезвоживания
Дегидратацией (или обезвоживанием) называют процесс потери в мягких тканях воды на фоне нарушенного обмена веществ. При инфицировании паратуберкулёзным энтеритом организм обезвоживается из-за диареи. Когда мягкие ткани теряют больше четверти водяных ресурсов корова гибнет.
На фоне дегидратации наблюдается возникновение таких признаков:
- постоянная жажда;
- угнетенное состояние;
- снижение объёма урины;
- судороги;
- после щипковой пробы складка на коже длительное время не выпрямляется;
- шерстяные покровы сухие, взъерошенные;
- ткани носогубного зеркальца сухие.
Обезвоживание у животного, зараженного болезнью Йоне, проявляется уже на последнем этапе заболевания.
Признаки кахексии
По внешним признакам кахексия похожа на дегидратацию, однако это состояние не сопровождается потерей воды из мягких тканей. В этом случае у животного снижается масса тела, атрофируются мышцы, отмечается появление слабости. При щипковой пробе не наблюдается признаков обезвоживания. Хотя чаще всего на фоне паратуберкулёзного энтерита отмечается совместное течение кахексии с дегидратацией.

Микобактериоз легких: основные сведения, причины, симптомы, методы лечения
 Какая клиническая картина характерна для заболевания.
Какая клиническая картина характерна для заболевания.
Микобактериоз легких относится к глубоким хроническим заболеваниям дыхательной системы. Это заболевание возникает по причине инфицирования организма атипичным типом микобактерий (нетуберкулезным).
Он может развиваться как самостоятельное заболевание или возникнуть на фоне активного туберкулеза. Согласно распространенному мнению микобактериоз не является опасной патологией, однако развитие такого заболевания дыхательной системы без своевременного лечения может приводить к тяжелым последствиям до летального исхода.
Симптомы течения паратуберкулеза
Период заражения (инкубации) от 1 месяца до нескольких лет. Специалисты выделяют латентную (скрытую) и открытую (клиническую) формы течения заболевания. Скрытая форма паратуберкулеза отличается отсутствием признаков болезни. Возможен переход данной формы течения болезни в клиническую форму. Чаще всего это происходит после отела (окота) животного. У животного наблюдается общая слабость, снижение удоя, потеря веса, температура тела стабильная, начинается понос. Кал жидкий, с обильной слизью, пузырьками газа и кровью. Болезнь истощает животное, оно не в состоянии стоять, наблюдается шилозадость. Болезнь может длиться несколько месяцев.
Представители рода микобактерий
По старой системе микобактерии классифицировались, в зависимости от их свойств и скорости роста на питательных средах. Однако более новая номенклатура базируется на кладистике.
Медленно растущие
Микобактерии туберкулёзного комплекса (MTBC)
Mycobacterium tuberculosis complex (MTBC) представители комплекса патогенны для человека и животных, и вызывают заболевание туберкулёз. Комплекс включает:
M. tuberculosis, наиболее опасен для человека, как возбудитель туберкулёза
M. bovis
M. bovis BCG
M. africanum
M. canetti
M. caprae
M. microti
M. pinnipedii
Микобактерии avium-комплекса (MAC)
Основная статья: MAC
Mycobacterium avium complex (MAC) — часть большой группы нетуберкулёзных микобактерий (НТМБ), виды, составляющие данный комплекс, патогенны для человека и животных, чаще вызывают диссеминированные процессы внелёгочной локализации и являлись ранее одной из основных причин смерти больных СПИДом. Комплекс включает:
M. avium
M. avium paratuberculosis
M. avium silvaticum
M. avium «hominissuis»
M. colombiense
Simiae-ветвь
- M. triplex
- M. genavense
- M. florentinum
- M. lentiflavum
- M. palustre
- M. kubicae
- M. parascrofulaceum
- M. heidelbergense
- M. interjectum
- M. simiae
Некатегоризированные
- M. branderi
- M. cookii
- M. celatum
- M. bohemicum
- M. haemophilum
- M. malmoense
- M. szulgai
- M. leprae, которая вызывает лепру
- M. lepraemurium
- M. lepromatosis, другая (менее распространенная) причина лепры
- M. africanum
- M. botniense
- M. chimaera
- M. conspicuum
- M. doricum
- M. farcinogenes
- M. heckeshornense
- M. intracellulare
- M. lacus
- M. marinum
- M. monacense
- M. montefiorense
- M. murale
- M. nebraskense
- M. saskatchewanense
- M. scrofulaceum
- M. shimoidei
- M. tusciae
- M. xenopi
Быстро растущие
Fortuitum-ветвь
- M. fortuitum
- M. fortuitum subsp. acetamidolyticum
- M. boenickei
- M. peregrinum
- M. porcinum
- M. senegalense
- M. septicum
- M. neworleansense
- M. houstonense
- M. mucogenicum
- M. mageritense
- M. brisbanense
- M. cosmeticum
Некатегоризированные
- M. confluentis
- M. flavescens
- M. madagascariense
- M. phlei
-
M. smegmatis
- M. goodii
- M. wolinskyi
- M. thermoresistibile
- M. gadium
- M. komossense
- M. obuense
- M. sphagni
- M. agri
- M. aichiense
- M. alvei
- M. arupense
- M. brumae
- M. canariasense
- M. chubuense
- M. conceptionense
- M. duvalii
- M. elephantis
- M. gilvum
- M. hassiacum
- M. holsaticum
- M. immunogenum
- M. massiliense
- M. moriokaense
- M. psychrotolerans
- M. pyrenivorans
- M. vanbaalenii
- M. pulveris
Некатегоризированные
- M. arosiense
- M. aubagnense
- M. caprae
- M. chlorophenolicum
- M. fluoroanthenivorans
- M. kumamotonense
- M. novocastrense
- M. parmense
- M. phocaicum
- M. poriferae
- M. rhodesiae
- M. seoulense
- M. tokaiense
морфология
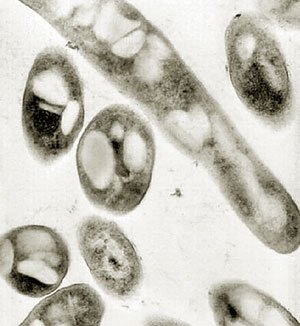
Бактерии, которые принадлежат к группе Mycobacterium avium комплекс Они имеют форму стержня с закругленными концами. Они не имеют каких-либо удлинений на клеточной поверхности, таких как реснички и жгутики. Они обычно встречаются как отдельные бактерии. Они не образуют шнуры или цепочки.
Они представляют собой клеточную стенку, которая состоит из трех листов, липофильного наружного слоя и базального слоя пептидогликана. Это связано через ковалентные связи с миколовой кислотой
Это важно, потому что именно это делает поверхность клетки гидрофобной и восковой
В культурах наблюдается, что колонии могут быть представлены двумя способами: прозрачные гладкие или непрозрачные с формой свода.
Что касается его генетического материала, он состоит из одной круглой хромосомы, в которой содержатся все гены бактерий. ДНК бактерии имеет длину 5,575,491 нуклеотидов, в них преобладают нуклеотиды, образованные азотистыми основаниями гуанином и цитозином..
Аналогично, приблизительно 90% ДНК — это гены, которые кодируют экспрессию белков. В общей сложности эти бактерии синтезируют в общей сложности 5120 белков с самым разнообразным использованием.
Genome structure
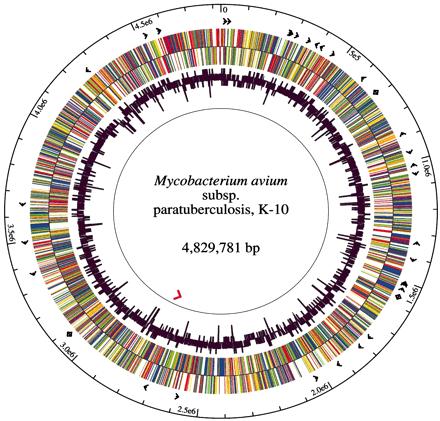
The Map strain used for sequencing, K-10, was originally isolated from a dairy herd in Wisconsin by investigators of the USDA National Animal Disease Center . This strain is a typical bovine type II clinical isolate which was chosen because of its high efficiency of transformation with plasmid DNA , its virulence and its amenability to transposition mutagenesis. By random shotgun sequencing, 1.8- to 3.0-kb fragments were cloned into pUC18 and 66,129 sequences were used to create the final genome assembly. As represented in the figure, the K-10 Map genome has a single circular chromosome of 4,829,781 base pairs, 91.3% of which are protein coding. Map has a GC (guanine cytosine) content of 69.3%, an average gene density of 1,112 base pairs per gene and an average gene length of 1,015 base pairs. This genome encodes 4,350 ORFs, 45 tRNAs and 1 rRNA operon. 39 protein sequences were found within the Map genome which have no identifiable homolog recorded as of yet. About 1.5% of the Map genome consists of repetitive DNA .
Of the 19 insertion sequences identified in the K-10 genome, most represent homologs of other Mycobacterium IS elements. IS_MAP02 and IS_MAP04 are of interest because they have no homologs in other mycobacteria and thus could possibly be used as specific diagnostic targets for Map. The Map genome encodes for all proteins involved in the following metabolic pathways: glycolysis, the pentose phosphate pathway, the tricarboxylic acid cycle, and the glyoxalate cycle. Also, the large number of genes for regulatory function found within the genome is consistent with Map’s ability to survive in a wide range of environmental conditions. One major difference between Map and other mycobacteria is its inability to produce mycobactin in vitro, which is a siderophore responsible for the binding and transport of iron into the cell. A sequence comparison of the mycobactin gene cluster between Map K-10, M. avium strain 104 and M. tuberculosis strain H37Rv reveals a possible reason for this deficiency. Within this cluster, the mbtA gene is much shorter in Map than the other two, lacking more than 200 residues important for protein function. Though this needs to be tested more thoroughly, this truncated domain may be the limiting factor in mycobactin production for Map since MbtA has been found to initiate siderophore synthesis. One additional Map genome feature to note is the extentsive functional redundancy; a result of gene duplication, this redundancy is based on amino acid content and is usually high among genes involved in lipid metabolism and oxidoreduction . A greater concentration of proteins for lipid metabolism in Map compared to other species may reflect its requirement of a robust cell wall which allows it to survive and colonize in the ruminant intestine .
Pathophysiology
MAP causes Johne’s disease in cattle and other ruminants. It has long been suspected as a causative agent in Crohn’s disease in humans, but studies have been unable to show definite correlation.
Recent studies have shown that MAP present in milk can survive pasteurization, which has raised human health concerns due to the widespread nature of MAP in modern dairy herds. MAP survival during pasteurization is dependent on the D72C-value of the strains present and their concentration in milk. It is heat resistant and is capable of sequestering itself inside white blood cells, which may contribute to its persistence in milk. It has also been reported to survive chlorination in municipal water supplies.
MAP is a slow growing organism and is difficult to culture. Bacterial cultures were regarded as Gold standards for detection of MAP. Detection is very limited in fresh tissues, food, and water. Recently, John Aitken and Otakaro Pathways have discovered a method to culture MAP from human blood. Testing is ongoing. Professor John Hermon-Taylor of Kings College London is developing a new vector type anti MAP vaccine which he claims is both curative and preventative. Stage 1 human trials began in January 2017 and concluded successfully in September 2019. He is also developing a companion MAP blood test.
It is not susceptible to antituberculosis drugs (which can generally kill Mycobacterium tuberculosis). MAP is susceptible to antibiotics used to treat Mycobacterium avium disease, such as rifabutin and clarithromycin, however the capacity of these antibiotics to eradicate MAP infection in vivo has not been established.
Crohn’s disease
MAP is recognized as a multi-host mycobacterial pathogen with a proven specific ability to initiate and maintain systemic infection and chronic inflammation of the intestine of a range of histopathological types in many animal species, including primates.
MAP has been found in larger numbers within the intestines of Crohn’s disease patients and in significant amount of irritable bowel syndrome patients compared to those suffering from ulcerative colitis or otherwise healthy controls. One study concluded that MAP «may act as a causative agent, have a role in the context of secondary infection, which may exacerbate the disease, or represent non-pathogenic colonisation.»
Как лечить животных, инфицированных паратуберкулезом
Лечить животное, у которого выявлена болезнь Йоне, бессмысленно, так как это неизлечимое заболевание. Все вольные особи с подтверждённым паратуберкулёзом подлежат изоляции с последующим убоем. Мясную продукцию можно использовать для приготовления еды. А вот от органов и тканей, пораженных инфекцией, придется избавиться.
Если у животного выявлена позитивная реакция на введение птичьего туберкулина, но отсутствуют клинические признаки патологии, его следует забить либо отправить в изолятор для инфицированных паратуберкулёзным энтеритом. Телят, родившихся от таких коров, можно оставить на откорм, но использовать в качестве воспроизводителей запрещено.

Диагностика болезни
Диагноз – паратуберкулез – ставят по эпизоотическим и клиническим признакам, по результатам аллергических проб и лабораторных бактериоскопических исследований на наличие возбудителя. Дополнительно применяют еще одно исследование – реакцию связывания комплемента.
Патологические изменения при паратуберкулезе затрагивают тонкий кишечник, его заднюю часть. Характерные симптомы – 5-10-кратное утолщение слизистой в местах поражения. Наблюдается сужение просвета кишки, хорошо заметное на поперечном разрезе. На продольном видна явная продольная и поперечная складчатость, при растягивании складки не исчезают. Лимфоузлы на брыжейке и илеоцекальном клапане увеличены, упругие, на разрезе влажные, серо-желтого цвета.

У некоторых больных животных может отмечаться отек серозной оболочки брыжейки и кишечника, увеличение лимфоузлов, частичное увеличение и частичное атрофирование кишечных ворсинок.